【化学—化学与技术】
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。
(1)工业上采用电解氧化铝和冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:2Al2O3 4Al+3O2↑。
4Al+3O2↑。
加入冰晶石的作用为_______________________。
(2)上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为________,下列可作阴极材料的是______。
a.铝材 b.石墨 c.铅板 d.纯铝
(3)阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式_______________________。在铝阳极氧化过程中,需要不断地调整电压,理由是_________________。
(4)下列说法正确的是__________________。
a.阳极氧化是应用原电池原理进行金属材料表面处理的技术
b.铝的阳极氧化可增强铝表面的绝缘性能
c.铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
d.铝的阳极氧化膜富多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
现有反应:mA(g) + nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1) 该反应的正反应为 ________反应(填吸热或放热),△S_____0 (填“>”、“=”或“<”),由此判断,此反应自发进行的条件为_______。
A 一定自发 B一定不自发 C高温自发,低温不自发 D低温自发,高温不自发
(2) 减压时,A的质量分数_________。(填“增大”、“减小”或“不变”,下同)
(3) 若加入B (体积不变),则A的转化率_________。
(4) 若升高温度,则平衡时B、C的浓度之比C(B) :C(C) 将_________。
(5) 若加入催化剂,平衡时气体混合物的总物质的量_______。
(6) 若B是有色物质,A、C均无色,则加入C (体积不变)后混合物颜色_______;(填“变深”、“变浅”或“不变”,下同)
(7)维持容器内压强不变,充入氖气后,混合物颜色。
(1)对于下列反应:2SO2 + O2 2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。
2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。
(2)下图表示在密闭容器中反应:2SO2+O2 2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。
2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。
①a b过程中改变的条件可能是;
②b c过程中改变的条件可能是;
③若加入催化剂,请将反应速度变化情况画在c~d处。
(3)请用化学平衡移动知识解释久置的氯水(尤其是长期放置在见光环境),最后浅黄绿色消失,溶液变成稀盐酸:
(5分)氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式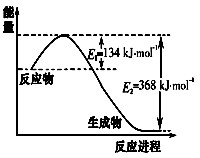
(2) 自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产。
请回答下列问题:
(1)已知:①N2(g)+O2(g)=2NO(g)△H1= +180.5kJ/mol
②N2(g)+3H2(g) 2NH3(g)△H2=-92.4kJ/mol
2NH3(g)△H2=-92.4kJ/mol
③2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ/mol
写出氨气经催化氧化生成一氧化氮气体和水蒸气的热化学方程式:
航天技术使用氢氧电池具有高能、轻便,不污染优点,氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式均可表示为:2H2+O2 ="==" 2H2O ,
酸式氢氧燃料电池的电解质是酸:
其负极反应为:2H2-4e-="==" 4H+,则正极反应为 ;
碱式氢氧燃料电池的电解质是碱,
其正极反应表示为:O2+2H2O+4e-= 4OH-,则负极反应为:。
(每空3分,共12分) A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。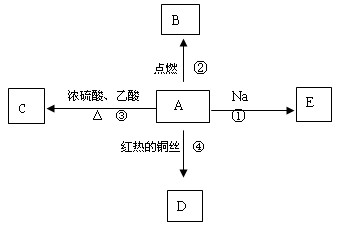
(1)写出A的结构式
(2)写出下列反应的化学方程式(有机物用结构简式表示):
反应①:
反应②:
反应④: