某研究小组以CaCl2和H2为原料,试图制备 +1价Ca的化合物,结果发现产物中只有两种化合物(甲和乙)。元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性。请回答下列问题:
(1)生成甲的化学反应方程式为 。
(2)甲与水反应可得H2,其化学方程式是 。
(3)在加热条件下,乙的水溶液(浓)与MnO2反应的离子方程式是 ;乙的水溶液与Fe反应所得的溶液不稳定,保存该溶液的措施是 。
(4)请写出一个你认为可能得到CaCl的化学方程式(以CaCl2为原料) 。
同学们,我们学习过的化学反应有很多了,让我们对所学过的化学反应方程式做个总结吧!有一些化学反应可用下式表示
A + B ─→ C + D + H2O
请你根据下面的提示回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程
式: 。
(2)若C为能使酚酞溶液变红的气体,则实验室制备C的方程式为 。
(3)若A为Na2O2,B为硫酸,则C和D的化学式是 。
(4)若A为红色固体,D能使品红褪色,反应的化学方程式为: 。
(5)若A非金属为单质,B为第二周期某种元素的最高价氧化物的水化物,请写出符合上式的化学方程式: 。
【化学—选修3:物质结构与性质】
绿柱石被国际珠宝界公认为四大名贵宝石之一。主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿。试回答下列问题:
(1)基态Al原子中,电子填充的最高能级是_______,基态Cr原子的价电子排布式是_____。
(2)用“>”或“<”填空:
| 第一电离能 |
键能 |
沸点 |
离子半径 |
| Be_____B |
C—C_____Si—Si |
H2S_____H2O |
Al3+_____O2- |
(3)BeCl2分子的空间构型是______,它的二聚体Be2Cl4结构如右图所示,其中Be原子的杂化方式是_____。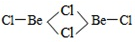

(4)强还原剂LiAlH4能将SiCl4还原成SiH4,试写出SiH4在空气中自燃的化学方程式______。
(5)Be的氧化物的立方晶胞结构如右图所示,已知氧化铍晶体的密度为ρg·cm-3,则晶胞连长为___cm(设NA为阿伏加德罗常数的值,用含NA、ρ的代数式表示)。
汽车尾气作为空气污染的主要来源之一,其中含有大量的有害物质,包括CO、NOx、碳氢化合物和固体悬浮颗粒等。对汽车尾气的治理使环境工作者面临了巨大的挑战。试回答下列问题:
(1)用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
②CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
则由CH4将NO2完成还原成N2,生成CO2和水蒸气的热化学方程式是____________________;
(2)NOx也可被NaOH溶液吸收而生成NaNO3、NaNO2,已知某温度下,HNO2的电离常数Ka=9.7×10-4mol•L-1,NO2-的水解常数为Kh=8.0×10-10mol•L-1,则该温度下水的离子积常数=______(用含Ka、Kh的代数式表示),此时溶液的温度______25℃(“>”、“<”、“=”)。
(3)化工上利用CO合成甲醇,反应的热化学方程式为:CO(g)+2H2(g) CH3OH(g)△H=-90.8KJ•mol-1。不同温度下,CO的平衡转化率如右图所示:图中T1、T2、T3的高低顺序是________,理由是______。
CH3OH(g)△H=-90.8KJ•mol-1。不同温度下,CO的平衡转化率如右图所示:图中T1、T2、T3的高低顺序是________,理由是______。
(4)化工上还可以利用CH3OH生成CH3OCH3。在体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g)。
CH3OCH3(g)+H2O(g)。
| 容器编号 |
温度(℃) |
起始物质的量(mol) |
平衡物质的量(mol) |
|
| CH3OH |
CH3OCH3 |
H2O |
||
| Ⅰ |
387 |
0.20 |
0.080 |
0.080 |
| Ⅱ |
207 |
0.20 |
0.090 |
0.090 |
该反应的正反应为________反应(填“吸热”、“放热”),若起始是向容器Ⅰ中充入CH3OH0.15mol、CH3OCH30.15mol和H2O0.10mol,则反应将向_____方向进行(填“正”、“逆”)。
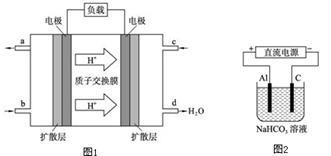
(5)CH3OH燃料电池在便携式通讯设备、汽车等领域有着广泛的应用。已知电池工作时的总反应方程式为:2CH3OH+3O2=2CO2+4H2O,电池工作时的示意图如右图所示:
质子穿过交换膜移向_____电极区(填“M”、“N”),负极的电极反应式为________。
MnO2是具有多种特殊功能的材料,工业上用菱铁矿(MnCO3)为原料制备MnO2的工业流程如下: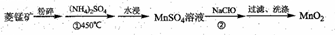
试回答以下问题:
(1)提高水浸效率的方法有______、______(填两种)。实验室里洗涤MnO2时用到的玻璃仪器有_____。NaClO的电子式为_________。
(2)反应①的化学方程式为___________。
(3)反应②生成MnO2的同时,得到一种黄绿色的气体,则该反应的离子方程式为__________。
(4)反应②的尾气常温下通入NaOH溶液后,生成NaClO可循环利用,若制得87gMnO2,理论上还需要补充NaClO______mol。
(5)工业上还可以将菱锰矿用硫酸直接浸取后,通过电解MnSO4和H2SO4的混合液制备MnO2,则电解时阳极的电极反应式为__________。
工业制硝酸的主要反应为:4NH3 (g) +5O2 (g)  4NO(g) + 6H2O(l)△H
4NO(g) + 6H2O(l)△H
(1)已知氢气的燃烧热为285.8kJ/mol。
N2(g)+3H2(g)═ 2NH3(g)△H = ﹣92.4kJ/mol;
N2(g)+ O2(g)═ 2NO(g)△H = +180.6kJ/mol。
则上述工业制硝酸的主要反应的△H= 。
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 浓度 |
c(NH3)(mol/L) |
c(O2)(mol/L) |
c(NO)(mol/L) |
| 起始 |
0.8 |
1.6 |
0 |
| 第2min |
0.6 |
a |
0.2 |
| 第4min |
0.3 |
0.975 |
0.5 |
| 第6min |
0.3 |
0.975 |
0.5 |
| 第8min |
0.7 |
1.475 |
0.1 |
①反应在第2min到第4min时,O2的平均反应速率为 。
②反应在第6min时改变了条件,改变的条件可能是 (填序号)。
A.使用催化剂B.升高温度C.减小压强D.增加O2的浓度
③下列说法中能说明4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g)达到平衡状态的是_________ (填序号)。
4NO(g) + 6H2O(g)达到平衡状态的是_________ (填序号)。
A.单位时间内生成n mol NO的同时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O) = 4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
(3)某研究所组装的CH3OH﹣O2燃料电池的工作原理如图1所示。
①该电池工作时,b口通入的物质为 。
②该电池正极的电极反应式为: 。
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图2所示)的过程中,发现溶液逐渐变浑浊并有气泡产生,其原因可能是 (用相关的离子方程式表示)。