【化学—选修3:物质结构与性质】
绿柱石被国际珠宝界公认为四大名贵宝石之一。主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿。试回答下列问题:
(1)基态Al原子中,电子填充的最高能级是_______,基态Cr原子的价电子排布式是_____。
(2)用“>”或“<”填空:
| 第一电离能 |
键能 |
沸点 |
离子半径 |
| Be_____B |
C—C_____Si—Si |
H2S_____H2O |
Al3+_____O2- |
(3)BeCl2分子的空间构型是______,它的二聚体Be2Cl4结构如右图所示,其中Be原子的杂化方式是_____。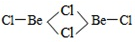

(4)强还原剂LiAlH4能将SiCl4还原成SiH4,试写出SiH4在空气中自燃的化学方程式______。
(5)Be的氧化物的立方晶胞结构如右图所示,已知氧化铍晶体的密度为ρg·cm-3,则晶胞连长为___cm(设NA为阿伏加德罗常数的值,用含NA、ρ的代数式表示)。
短周期元素X、Y、Z、L、M、Q的原子半径和主要化合价见下表
| 元素代号 |
X |
Y |
Z |
L |
M |
Q |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.099 |
0.077 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+6、-2 |
+7、-1 |
+4、-4 |
-2 |
就以上6种元素,用化学用语回答下列问题
(1)同主族的元素是 ,
(2)写出同周期元素间形成的常温下是有毒气体化合物的分子式为 ,
(3)写出不同周期的元素间形成的常温下为液体且难溶于水的任意一种化合物的电子式。
(4)等质量的X、Y的单质与足量盐酸反应,生成H2的物质的量之比为
(5)写出由表中元素形成的物质间发生常见的置换反应的化学方程式
开发使用清洁能源,发展“低碳经济”正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)甲烷水蒸气转化法制H2的主要转化反应如下:
CH4(g) + H2O(g) CO(g) + 3H2(g)△H=+206.2 kJ·mol-1
CO(g) + 3H2(g)△H=+206.2 kJ·mol-1
CH4(g) + 2H2O(g) CO2(g) + 4H2(g)△H=+165.0 kJ·mol-1
CO2(g) + 4H2(g)△H=+165.0 kJ·mol-1
上述反应所得原料气中的CO能使合成氨的催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是。
(2)生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0
①一定条件下CH4的平衡转化率与温度、压强的关系如图a。则A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为___________。(填“<”、“>”、“="”" );
②100℃时,将1 mol CH4和2 mol H2O通入容积为1 L的定容密封容器中,发生反应,能说明该反应已经达到平衡状态的是__________
a.容器内气体密度恒定
b.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
c.容器的压强恒定
d.3v正(CH4) = v逆(H2)
(3)25℃时,在20mL0.1mol/L氢氟酸中加入VmL0.1mol/LNaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是_____。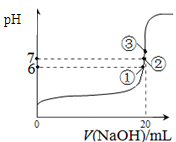
A.pH=3的HF溶液和pH=11的NaF溶液中, 由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(Na+)=0.1mol/L
(4)长期以来,一直认为氟的含氧酸不存在。1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H—O—F。HFO与水反应得到HF和化合物A,该反应的化学方程式为。
化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)“三酸”与“两碱”之间均可反应,酸过量时, 若用化学方程式表示有六个,若用离子方程式表示却只有两个,一个是H++OH-=H2O,请写出另一个离子方程式:。
(2) 实验室制备H2、CO2、NH3、SO2时,用盐酸和稀硫酸可制备的相同气体是_______。
(3)烧碱、纯碱溶液均可吸收CO2,当含0.1 mol NaOH的溶液吸收一定量CO2后,将溶液低温小心蒸干得到固体的组成可能有四种情况,分别是(填化学式):
①;②Na2CO3;③Na2CO3和NaHCO3;④NaHCO3。
(4)将(3)得到的固体重新溶解于水,向其中加入盐酸,调节溶液的pH恰好等于7,再将溶液蒸干,最终得到固体的质量为g。
(5)利用侯德榜制碱法可制两碱的一种,请写出制取小苏打时在溶液中发生反应的总化学方程式。
植物精油具有抗菌消炎、解热镇痛等药物功效。从樟科植物枝叶中提取的精油中含有甲、乙、丙三种成分。
Ⅰ.甲经下列过程可转化为乙
(1)反应①的反应类型为。
(2)乙的结构简式为,1mol乙最多可与mol H2反应。
Ⅱ通过下列合成路线由乙可得到丙(部分反应产物略去)
已知下列信息: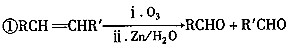
②丙的分子式为C16H14O2,能与溴水、NaOH溶液反应。
(3)A的名称是。B→C的反应条件为。
(4)乙与新制Cu(OH)2反应的化学方程式为。
写出同时符合下列要求的D的同分异构体的结构简式:。
属于二取代苯
b.分子中有5种不同化学环境的氢原子,其个数之比为1:2:2:1:2
c.能使溴的CCl4溶液褪色,且在酸性条件下可以发生水解反应
叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O=NaN3+NaOH+NH3,3NaNH2+NaNO3=NaN3+3NaOH+NH3↑。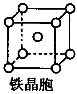
回答下列问题:
(1)氮所在的周期中,电负性最大的元素是________,第一电离能最小的元素是_______。
(2)基态氮原子的L层电子排布图为_______________。
(3)与N3-互为等电子体的分子为__________(写出一种)。依据价层电子对互斥理论,NO3-的空间构型为_____________。
(4)氨基化钠(NaNH2)和叠氮化钠(NaN3)的晶体类型为_________________。叠氮化钠的水溶液呈碱性,用离子方程式表示其原因:_____________________________。
(5)N2O沸点(-88.49℃)比NH3沸点(-33.34℃)低,其主要原因是__________________。
(6)安全气囊的设计原理为6NaN3+Fe2O3 3Na2O+2Fe+9N2↑。
3Na2O+2Fe+9N2↑。
①氮分子中σ键和π键数目之比为________________________。
②铁晶体中存在的化学键类型为__________________________。
③铁晶体为体心立方堆积,其晶胞如图所示,晶胞边长为a cm,该铁晶体密度为___________(用含a、NA的表达式表示,其中NA为阿伏加德罗常数)。