Ⅰ.已知A、B、C、D四种分子所含原子的数目依次为1、3、6、6,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1:2。D是一种有毒的有机物。
(1)组成A分子的原子的元素符号是 ;
(2)从B分子的立体结构判断,该分子属于 分子(填“极性”或“非极性”);
(3)C分子中都包含_______个σ键,_______个π键;(2分,每空1分)
(4)D的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明D是何物质):
__________________________________________________ ____。
Ⅱ.CO的结构可表示为C≡O,N2的结构可表示为N≡N。
(5)下表是两者的键能数据:(单位:kJ/mol)
| |
A-B |
A=B |
A≡B |
| CO |
357.7 |
798.9 |
1071.9 |
| N2 |
154.8 |
418.4 |
941.7 |
结合数据说明CO比N2活泼的原因:________________________________。
Ⅲ.(6)基态Ni原子的核外电子排布式为 。
IV.(7)Cu3N的晶胞结构如图,N3-的配位数为__________。
写出下列物质的电子式
H2O 1KOH 2
CO2: 3Na2O2: 4
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图所示的转化关系,已知C为密度最小的气体。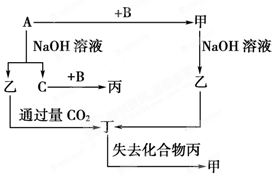
根据图示转化关系回答:
(1)写出下列物质的化学式:B、丙、丁。
(2)组成单质A的元素在周期表中的位置是。
(3)乙与过量CO2反应的离子反应方程式____________________________
(4)A与NaOH溶液反应的化学反应方程式____________________________
已知A、B、C、D四种短周期元素在元素周期表中的相对位置如下图所示,它们的原子序数之和为46。请填空: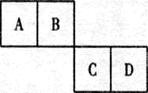
(1)B元素的名称为D元素的原子结构示意 图为。
(2)B有多种氧化物,其中之一是一种无色气体。该气体在空气中会迅速变成红棕色,在一定条件下,4L的该无色气体与3L的氧气相混合,被足量的水完成吸收,且只生成一种B的含氧酸,该含氧酸的化学式为 。
(3)离子半径:D﹣C2﹣(填“>”、“<”、“=”)。还原性:D﹣C2﹣(填“>”、“<”、“=”)。
欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。(已知:碳酸不能溶解Al(OH)3沉淀)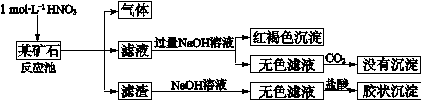
(1)用滤渣制备粗硅的化学反应方程式为
(2)下列说法正确的是
a.酸性:H2CO3>H2SiO3b.结合质子的能力:CO> AlO2->HCO3-
c.稳定性:H2O>CH4>SiH4d.离子半径:O2-<Al3+
(3)滤渣和NaOH溶液反应的离子方程式是
通过现象说明此矿山中不含Al2O3
(4)该矿石和稀HNO3发生氧化还原反应的离子方程式为
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,主要两个目的是,;
若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg ,理论上至少需要1 molL-1 HNO3的体积为L。
某校学生化学实验小组,为验证Cl2氧化性强于硫和N2,设计了一套实验装置:
(部分夹持装置已略去)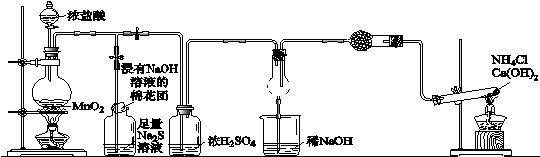
A B C D E
(1)写出A中反应的离子方程式
(2)B中出现黄色浑浊现象,产生此现象的离子方程式
(3)D中干燥管中出现的现象为
产生的NH3过量,则D干燥管发生化学方程式为
(4)有同学认为D中的现象并不能说明Cl2氧化性强于N2,需要在C之前加装洗气装置,请画出
其装置图(并注明盛装试剂)。
(5)证明非金属性Cl > S,用另一种相关事实说明