高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是。
| A.铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+ |
| B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10-15,在AB2、AC均为饱和的混合液中,测得c(B-)=1.6×10-3 mol·L-1,则溶液中c(C2-)为()
A.1.8×10-13 mol·L-1 B.7.3×10-13 mol·L-1
C.2.3 mol·L-1 D.3.7 mol·L-1
室温下,下列各组离子在指定溶液中能大量共存的是()
| A.饱和氯水中:Cl-、NO3-、Na+、SO32- |
B.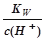 =10-13mol·L-1 溶液中:NH4+、Mg2+、NO3-、SO42- =10-13mol·L-1 溶液中:NH4+、Mg2+、NO3-、SO42- |
| C.通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- |
| D.Na2S溶液中:SO42-、K+、Cl-、Cu2+ |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2下列有关该电池的说法不正确的是
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C.电池充电过程中,阴极附近溶液的pH降低 |
| D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是
A.在0.1mol·L-1NaHCO3溶液中:c(Na+) c(HCO3-) c(HCO3-) c(CO32-) c(CO32-) c(H2CO3) c(H2CO3) |
| B.在0.1mol·L-1Na2CO3溶液中:c(OH-)- c(H+)= c(HCO3-)+2c(H2CO3) |
| C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1mol·L-1NaOH溶液:c(CO32-)> c(HCO3-)> c(OH-)> c(H+) |
| D.常温下,CH3COONa和CH3COOH混合溶液(pH="7," c(Na+)=0.1mol·L-1):c(Na+)= c(CH3COO-)=c(CH3COOH)> c(H+)= c(OH-) |
下列反应中,属于取代反应的是
①CH3CH=CH2+Br2 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH  CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3 C6H5NO2+H2O
C6H5NO2+H2O
| A.①② | B.③④ | C.①③ | D.②④ |