在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
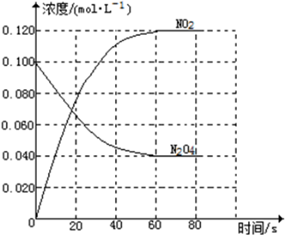
(1)反应的△H 0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为 mol·L-1·s-1反应的平衡常数K1为 。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10s又达到平衡。
①T 100℃(填“大于”“小于”),判断理由是 。
②列式计算温度T是反应的平衡常数K2
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向 (填“正反应”或“逆反应”)方向移动,判断理由是 。
(共8分)
(1)有反应:2NO2 N2O4 △H<0,根据图像判断后填空:
N2O4 △H<0,根据图像判断后填空:
|


(共10分)在一定条件下,将3molA 和1mol B 两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+ 2D(g)。2min末该反应达到平衡,生成0.8mol D ,并测得C的浓度为0.2mol·L-1。请填空:
xC(g)+ 2D(g)。2min末该反应达到平衡,生成0.8mol D ,并测得C的浓度为0.2mol·L-1。请填空:
(1)x=__________
(2)温度降低,平衡向右移动,则正反应是_____(填“放热”或“吸热”)反应。
(3)B的转化率为_________。
(4)能判断该反应达到平衡状态的依据是________(填编号)
A. 混合气体的密度不变
B. 容器中的压强不再变化
C. 生成D的反应速率是生成B的反应速率的2倍
D. 单位时间内生成3molA,同时生成1molB
(5)2min内平均速率v(A)=____________________________________。
(共6分)在一定条件下,反应xA 十yB  zC达到平衡。
zC达到平衡。
(1)若A、B、C都是气体,在增压后平衡向逆反应方向移动,则x,y,z之间的关系是。
(2)若C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则A的转化率将(填“增大”、“减小”或“不变”)
(3)若A为固体,B、C为气体,且y>z,则增大压强时混和气体的平均相对分子质量将(填“增大”“减小”或“不变”)
在水溶液中橙色的Cr2O72-与黄色的CrO42-有平衡关系:Cr2O72- + H2O  2CrO42-+ 2H+,把重铬酸钾溶于水配成稀溶液呈橙色。
2CrO42-+ 2H+,把重铬酸钾溶于水配成稀溶液呈橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈色。
(2)向已加入NaOH溶液的溶液中再加入过量稀硫酸,则溶液应是色,因为。
(3)向原溶液中加入硝酸钡溶液(已知BaCrO4为黄色沉淀),则平衡(向左移或向右移),溶液颜色将。
2,3-二氧呋喃是抗肿瘤药物的中间体,四氢呋喃是常用溶剂,它们可以通过下列反应流程来合成: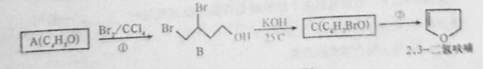
已知: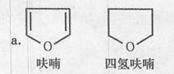
b.在碱存在的条件下,卤代烃可与酵发生如下反应:
R—X+R′—OH→R—O—R′+HX
请填写下列空白:
(1)化合物B的名称为;反应①的反应类型是;反应②的反应条件是。
(2)写出结构简式:A为;C为;A与乙酸反应生成的酯为。
(3)工业上可由二元醇D( C4H10O2)在一定条件下脱水制得四氢呋喃,该反应的化学方程式为。
(4)写出满足下列条件的呋喃的一种同分异构体的结构简式。
I.没有支链,且一元取代产物只有两种。
Ⅱ.不能与银氨溶液发生银镜反应。
Ⅲ.核磁共振氢谱图有2个峰,其面积之比为1:3。
(5)2,3—二氢呋喃在一定的条件下可以转变成四氢呋喃,如何用简单的化学方法检验2,3-二氢呋喃是否完全转化?。