【原创】在一定温度的密闭容器中将氨气充入容器中,进行如下的反应:2NH3 N2+3H2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NH3)=0.6 mol/L,c(N2)=0.2 mol/L。试求:
N2+3H2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NH3)=0.6 mol/L,c(N2)=0.2 mol/L。试求:
(1)氨气的转化率为多少?
(2)反应前后的压强比为多少?
(3)计算该温度下氮气的体积分数.
(4)在这5分钟内,用N2来表示的平均反应速率是多少?
(5)平衡时氢气的浓度是多少?
在500℃容积为2升的密闭容器中充入SO2和O2,其中SO2的浓度为1mol/L,经10秒后,达到平衡,2SO2(g)+O2(g) 2SO3(g),此时容器中SO3的浓度为0.9mol/L,O2的物质的量为2.1mol,试求:① SO2的转化率;② O2的起始浓度(mol/L);③ SO2的平均反应速率(mol/L· min)
2SO3(g),此时容器中SO3的浓度为0.9mol/L,O2的物质的量为2.1mol,试求:① SO2的转化率;② O2的起始浓度(mol/L);③ SO2的平均反应速率(mol/L· min)
把 3mol A 和 2.5mol B 混合于 2L 的密闭容器中,使它们发生反应:
3A(气) + B(气)  xC(气) + 2D(气)
xC(气) + 2D(气)
经5min后达到平衡生成1mol D,并测定C的平均速率为0.1 mol/L·min,则此反应中的B的转化率为________,C的系数为_______________,A的平衡浓度为_____________。
20%,2, 0.75 mol /L
已知下列两个热化学方程式:
H2(g)+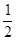 O2(g)==H2O(l) ΔH="-285" kJ/mol
O2(g)==H2O(l) ΔH="-285" kJ/mol
C3H8(g)+5O2(g)==3CO2(g)+4H2O(l)ΔH="-2" 220.0 kJ/mol
(1)实验测得H2和C3H 8的混合气体共5 mol,完全燃烧生成液态水时放热6 264.5 kJ,则混合气体中H2和C3H8的体积比是
(2)已知:H2O(l)==H2O(g)ΔH="+44.0" kJ/mol
写出丙烷燃烧生成CO2和气态水的热化学方程式。
0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态二氧化二碳和液态水,放出649.5kJ热量,其热化学反应方程式为:
又知H2O(l)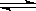 H2O(g);△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是J。
H2O(g);△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是J。
在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)(mol) |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)NO的平衡浓度c(NO)=。
(2)用O2表示从0~2s内该反应的平均反应速率v= 。
(3)下图中表示NO2变化的曲线是
(4)800℃时,容器内起始压强和平衡后压强之比为___________________