[实验化学]工业上常用水杨酸与乙酸酐反应制取解热镇痛药阿司匹林(乙酰水杨酸)。
【反应原理】

【物质性质】
| 试剂 |
沸点(℃) |
溶解度 |
化学性质 |
| 水杨酸 |
211 |
微溶于冷水,易溶于热水 |
|
| 乙酸酐 |
139 |
在水中逐渐分解 |
|
| 乙酰水杨酸 |
|
微溶于水 |
与碳酸钠反应生成水溶性盐 |
【实验流程】
(1)物质制备:向125 mL的锥形瓶中依次加入4 g水杨酸、10 mL乙酸酐(密度为1.08g/mL)、0.5 mL浓硫酸,振荡锥形瓶至水杨酸全部溶解,在85℃~90℃条件下,用热水浴加热5~10 min。
①加入水杨酸、乙酸酐后,需缓慢滴加浓硫酸,否则产率会大大降低,其原因是 。
②控制反应温度85℃~90℃的原因 。
(2)产品结晶:取出锥形瓶,加入50 mL蒸馏水冷却。待晶体完全析出后用布氏漏斗抽滤,再洗涤晶体,抽干。简要叙述如何洗涤布氏漏斗中的晶体? 。
(3)产品提纯:将粗产品转移至150 mL烧杯中,向其中慢慢加入试剂X并不断搅拌至不再产生气泡为止。进一步提纯最终获得乙酰水杨酸3.6 g。
①试剂X为 。
②实验中乙酰水杨酸的产率为 (已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180)。
(4)纯度检验:取少许产品加入盛有5 mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色,其可能的原因是 。
氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制的流程: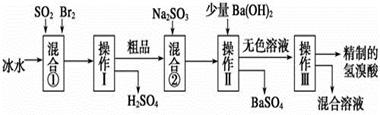
根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为______________________________________。
(2)混合①中使用冰水的目的是_________________________________。
(3)操作Ⅱ和Ⅲ的名称分别是________、__________。操作Ⅲ一般适用于分离_______混合物(选填编号)。
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中加入Na2SO3的目的是____________________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)常带有淡淡的黄色。于是甲、乙两同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为____________,若假设成立可观察到的现象为____________________________。乙同学假设工业氢溴酸呈淡黄色是因为_____________________________,其用于证明该假设所用的试剂为______________。
某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 |
溶液中检测出的物质 |
| 第一次 |
KCl、K2SO4、Na2CO3、NaCl |
| 第二次 |
KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 |
Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第__________次检测结果不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的 溶液(填化学式),其目的是检验CO32-
并将其除去;
第二步:加入溶液(填化学式),其目的是;
第三步:过滤,再向滤液中加入_____________溶液(填化学式),其目的是;
实验室欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制200mL 1.0 mol/L硫酸溶液:
(2)该实验室只备有①100 mL、②150 mL、③250 mL、④500 mL四种规格容量瓶,你认为应选用的容量瓶是(填写编号)。
(2)需要量取mL浓硫酸(保留一位小数)。
(3)该学生配制的操作过程如下:
①用量筒准确量取一定体积的浓硫酸,倒入适量小烧杯中;
②将适量蒸馏水慢慢倒入上述烧杯中并不断搅拌,冷却至室温;
③将烧杯中的溶液沿玻璃棒倒入选定的容量瓶中;
④用少量蒸馏水洗涮小烧杯1~2次,将洗涤液沿玻璃棒均转入容量瓶中;
⑤将蒸馏水沿玻璃棒倒入容量瓶中,至液面距离刻度线1~2cm为止;
⑥改用胶头滴管滴加蒸馏水,至凹液面最低处与刻度线相切;
⑦盖好瓶塞,上下翻转摇匀。
上述操作中你认为不正确或不合理的是(填序号)。
若用胶头滴管滴入水时,不小心滴过了刻度线,你认为应该采取的处理方法是:。
某同学配制1000mL 1.00mol/L NaCl溶液的步骤如下:
①用托盘天平称取58.5g NaCl固体并全部移入烧杯中;
②在上述烧杯中加入适量的蒸馏水,搅拌至NaCl固体全部溶解,冷却至室温;
③将烧杯中的溶液倾倒至容量瓶中;
④将蒸馏水注入容量瓶至刻度线下1cm~2cm;
⑤用胶头滴管滴加蒸馏水至液面与刻度线相切;
⑥盖好瓶塞,反复上下颠倒摇匀;
⑦静置后因液面低于刻度线再用胶头滴管滴加蒸馏水至液面与刻度线相切。
你认为上述步骤中不合理或不正确的是(填写序号)
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)烧杯间填满碎纸条的作用是。
(3)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等、不相等”),所求中和热(填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”)。