I.一定条件下铁可以和CO2发生反应:
Fe(s)+CO2(g) FeO(s)+CO(g) △H>0。1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
FeO(s)+CO(g) △H>0。1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。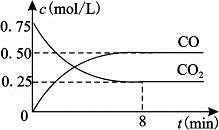
(1)8分钟内,CO的平均反应速率v(CO)=___________(结果保留3位有效数字)。
(2)1100℃时该反应的平衡常数K= (填数值);该温度下,若在8分钟时CO2和CO各增加0.5mol/L,此时平衡 移动(填“正向”、“逆向”或“不”)。
(3)1100℃时,2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 |
甲 |
乙 |
| 反应物投入量 |
3molFe、2molCO2 |
4molFeO、3molCO |
| CO的浓度(mol/L) |
C1 |
C2 |
| CO2的体积分数 |
φ1 |
φ2 |
| 体系压强(Pa) |
P1 |
P2 |
下列说法正确的是___________(填序号);
A.2C1 = 3C2 B.φ1 = φ2 C.P1<P2
II.(4)已知:①Fe(OH)3(aq) Fe3+(aq)+3OH-(aq);ΔH=" a" kJ•mol-1
Fe3+(aq)+3OH-(aq);ΔH=" a" kJ•mol-1
②H2O(l) H+(aq)+OH-(aq);ΔH="b" kJ•mol-1
H+(aq)+OH-(aq);ΔH="b" kJ•mol-1
请写出Fe3+发生水解反应的热化学方程式: 。
(5)柠檬酸(用H3R表示)可用作酸洗剂,除去水垢中的氧化铁。
溶液中H3R、H2R-、HR2--、R3-的微粒数百分含量与pH的关系如图所示。图中a曲线所代表的微粒数的百分含量随溶液pH的改变而变化的原因是 (结合必要的方程式解释)。调节柠檬酸溶液的pH=4时,溶液中上述4种微粒含量最多的是 (填微粒符号)。
III.(6)高铁酸钠(Na2FeO4)广泛应用于净水、电池工业等领域,工业常用电解法制备,其原理为
Fe+2OH--+2H2O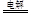 FeO42--+3H2↑
FeO42--+3H2↑
请设计一个电解池并在答题卡的方框内画出该装置的示意图并作相应标注。
其阳极反应式为:________________________________。
用一种试剂除去下列各物质中的杂质(括号内的物质)。写出所用试剂及反应的离子方程式。
(1)BaCl2(HCl):试剂 ,离子方程式 。
(2)O2(CO2):试剂 ,离子方程式 。
(3)SO42-(CO32-):试剂 ,离子方程式 。
(4)Cu粉(Al粉):试剂 ,离子方程式 。
实验室用密度为1.84g·cm-3,溶质的质量分数为98%的硫酸,配制250mL物质的量浓度为0.46mol·L-1的硫酸。
(1)98%的浓硫酸的物质的量浓度为 。
(2)现有下列几种规格的仪器,应选用 (用序号填空)。
①10mL量筒 ②50 mL量筒 ③100mL量筒 ④100mL容量瓶 ⑤250mL容量瓶
(3)容量瓶上标有 、 和 。
(4)下列操作使所配溶液的物质的量浓度偏高的是 。
| A.往容量瓶中转移溶液时有少量液体溅出 | B.未洗涤稀释浓H2SO4的小烧杯 |
| C.定容时俯视刻度线 | D.洗净容量瓶未干燥即用来配制溶液 |
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(1)8g CH4共有 mol氢原子,0.1molNH3共有约 个原子,同温同压下,同体积的NH3和H2S气体的质量比为 ;同温同压下,同质量的NH3和H2S气体的体积比为__ __。
(2)在标准状况下,15g某气体的分子数与11.2L CO的分子数相等,则该气体的摩尔质量为 。
(3)V L Fe2(SO4)3溶液中含Fe3+m g,则该溶液中Fe3+的物质的量浓度为_____ mol·L-1,溶质的物质的量浓度为______ mol·L-1。
(4)用脱脂棉包住约0.2g过氧化钠粉未,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉燃烧起来。由实验现象所得出的有关过氧化钠和水反应的结论是:a:有氧气生成;b Na2O2和水反应的化学方程式是 。
(12分)以下12种物质为中学化学中常见的物质:
①Cu②KCl③NaHSO4④SO3⑤H2SO4⑥C2H5OH(酒精)
⑦CaCO3 ⑧BaSO4 ⑨Cu(OH)2 ⑩Fe(OH)311NaOH 12 CaO
请按下列要求回答(填写物质的标号):
(1)属于电解质的是 。
(2)在水溶液中能电离出H+的是 ,属于酸的是 。
(3)属于碱的是 ,其中难溶性碱为 。
(4)难溶性盐是 。
为除去粗盐中的Ca2+、Mg2+、SO以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):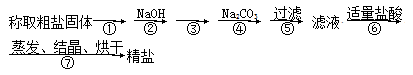
(1)步骤①的操作名称是 ,需要用到的仪器有______________、__________________。
(2)第③步中,加入的试剂是__________________(填化学式),判断该试剂已过量的方法是 。
(3)第④步中涉及反应的离子方程式 、 。
(4) 若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是 。