小明和小芳在讨论“能否用蜡烛燃烧法来粗略测定空气中氧气的含量”这一问题时,小芳认为:通过图1装置,用蜡烛燃烧法测得的空气中氧气的含量会 (填“偏高”、“偏低”或“不变”)。她根据蜡烛燃烧产物的特点阐述了自己的理由: ,并用图1装置进行实验,证实了自己的结论。(注:本题实验中装置的气密性良好,水槽中的液体是水。)
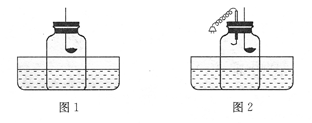
小明认真分析了小芳的实验结果后,进行了如下探究:
【提出问题】导致小芳这一实验结果还有其他原因吗?
【实验探究】小明设计了图2装置,进行以下操作:
(1)取黄豆粒大小的白磷,用滤纸吸去表面水分,放入捆在电烙铁下面贴片的凹槽内。
(2)将燃烧匙内的蜡烛点燃后迅速插入钟罩内,并立即塞紧橡皮塞。
(3)待蜡烛熄灭后(蜡烛有剩余),接通电烙铁电源,发现白磷先熔成液体,接着燃烧产生大量白烟,说明通电前钟罩内含有 ,产生白烟的文字表达式是 。
【得出结论】导致小芳这一实验结果的另一原因是 。
【交流与反思】小明和小芳分析了上述实验后,又提出了一个问题:能否用铁丝燃烧测定空气中氧气的含量,你的观点是 (填“能”或“否”),理由是 。
为探究一瓶久置的氢氧化钠溶液(原溶质质量分数16%)是否变质,同学们提出了多种方案,其中一种方案设计如下:
【查阅资料】:氢氧化钠溶液与空气接触可能发生的反应:
2NaOH+CO 2═Na 2CO 3+H 2O
Na 2CO 3+CO 2+H 2O═2NaHCO 3
NaOH与NaHCO 3在溶液中发生反应:
NaOH+NaHCO 3═Na 2CO 3+H 2O
【假设猜想】:1.该溶液未变质,溶质成分只有NaOH
2.该溶液已变质,…
【实验探究】:向一定质量的洁净烧杯中加入m 1g该氢氧化钠溶液,再加入溶质质量分数为20%硫酸m 2g(硫酸 足量),充分反应、冷却后称量.根据溶液总质量m判断该氢氧化钠溶液是否变质.
试结合该方案,回答下列问题:
(1)进行上述实验使用的称量仪器名称是 ,称量时,烧杯应放在该仪器的 盘.
(2)实验探究中,烧杯内溶液总质量m与氢氧化钠溶液是否变质的对应关系是:
m<(m 1+m 2)g,猜想 成立;m=(m 1+m 2)g,猜想 成立.
(3)补充完善猜想2:如果该溶液部分变质,溶质的成分为 (填化学式,下同);
如果该溶液完全变质,溶质成分可能为Na 2CO 3或NaHCO 3或 .
某化学兴趣小组把金属钠放到硫酸铜溶液中,实验并非如想象的有红色铜析出,而是生成一种蓝色沉淀,同学们非常好奇进行实验探究.
(1)【提出问题】金属钠放到硫酸铜溶液中到底发生了怎样的化学反应?
(2)【查阅资料】钠是非常活泼的金属,能与水发生剧烈反应,并放出气体,生成的溶液显碱性
(3)【实验探究】
实验一:把一小块擦干净的金属钠放到装有少量蒸馏水的试管中,点燃生成的气体,听到“噗”的一声后燃烧起来,说明有 气体生成
实验二:在剩余的溶液中滴加硫酸铜溶液,发现有蓝色沉淀
(4)【实验总结】实验一中发生反应的化学方程式是 ;实验二中发生反应的化学方程式是
(5)【实验拓展】兴趣小组又将一小块擦干净的金属钠放入盛有FeCl3溶液的烧杯中,观察到发生了化学反应,该反应的化学方程式是 .
某学习小组用下列装置进行CO2的制取及性质探究实验。
资料卡片:20℃时,碳酸钠在乙醇中几乎不溶解,氢氧化钠在乙醇中的溶解度为17.3g。20℃时,碳酸钠、碳酸氢钠在水中的溶解度分别为21.8g和9.6g。请根据如图回答下列问题:
(1)图中装置A是用大理石制CO2的装置,仪器a的名称是 ;装置A中发生反应的化学方程式是 ,在b处检验是否有CO2逸出的操作是 。
(2)装置C中放有干和湿的pH试纸各一张,当通入CO2一段时间后,湿pH试纸显示pH约为6,干pH试纸显示pH仍为7,实验结论是 。
(3)当通入CO2一段时间后,装置D中观察到溶液中有白色沉淀(NaHCO3)出现,则反应的化学方程式是
(4)当通入CO2一段时间后,装置E中观察到的实验现象是 ,则发生反应的化学方程式是 。

某化学兴趣小组的同学在实验室发现以前用的一瓶氢氧化钠溶液忘记了盖瓶塞,他们取这种氢氧化钠溶液少量于试管中,再逐滴加入稀盐酸,观察到有气泡产生.小组中有同学断定,这瓶氢氧化钠溶液已经变质.辅导老师肯定了该同学的看法,又有同学提出:所用氢氧化钠溶液是否完全变质?兴趣小组的同学在辅导老师的鼓励下又进行了如下的实验探究:
【提出问题】氢氧化钠溶液是否完全变质?
【进行猜想】(1)该氢氧化钠溶液部分变质;(2)该氢氧化钠溶液全部变质.
【查阅资料】氯化钡溶液呈中性.
【设计并进行实验】
|
实验步骤 |
实验现象 |
实验结论 |
|
(1)取少量该瓶氢氧化钠溶液于水管中,向溶液中滴加过量的BaCl2溶液,并不断振荡 |
有 产生 |
说明原溶液中一定有碳酸钠 |
|
(2)取步骤(1)试管中的少量上层清液,向其中滴加酚酞试液 |
发现溶液变红色 |
说明原溶液中一定有 . |
【结论】该小组同学所用的氢氧化钠溶液是 (填“部分”或者“全部”)变质.
【反思】氢氧化钠溶液露置于空气中容易变质,反应的化学方程式为: .
某学习小组查阅资料发现:H2O2能与Cl2发生反应Cl2+H2O2=2HCl+O2.小组讨论后认为只需证明生成了氧气,即可证明该结论,于是设计了如图所示的实验装置进行实验(夹持装置略去).
已知:(1)试管A中加入5mL30%的双氧水,试管B中几乎盛满10%NaOH溶液.
(2)Cl2是黄绿色气体,有毒.Cl2易与NaOH溶液反应:Cl2+2NaOH=NaCl+NaClO(次氯酸钠)+H2O
请回答下列问题:
(1)打开止水夹1、止水夹2,快速通入氯气排尽装置内的空气后,关闭止水夹2,继续缓缓通入氯气.判断装置内的空气已排尽的方法是 .
(2)试管B中NaOH溶液的主要作用是 .
(3)反应一段时间后试管B中的现象为 .检验试管B中气体的方法是:关闭止水夹1, .
(4)有的同学对实验中C试管中的气体来源产生质疑,你认为可能的来源是 (用化学方程式回答).对于质疑可以采用对比实验来解决.
