南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源。
(1)海水制盐。从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:
a.加过量的Ba(OH)2溶液;
b.加稍过量的盐酸;
c.加过量的Na2CO3溶液;
d.过滤;
e.蒸发。
正确的操作顺序是 (填字母)。加Na2CO3溶液的作用是除去 。
(2)海水淡化。下图是一个简易的蒸馏法淡化海水的装置。证明得到的水是淡水的方法是 。

(3)海水制镁。从海水中提取金属镁的过程如下图所示:
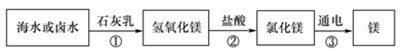
在上述转化过程中发生中和反应的是 (填反应顺序号)。海水中本身就含有氯化镁,则①、②两步的作用是 。
(4)海水“制碱”。氨碱法制纯碱是先通过化学反应生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱。
①氨碱法制纯碱中生成NaHCO3和NH4Cl的化学方程式为 ;
②反应中生成NaHCO3和NH4Cl的质量比为84∶53.5,NaHCO3和NH4Cl的溶解度曲线如图所示。

请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是 。
指出如图所示倾倒液体操作中的错误:
(1)____________________________________________________;
(2)____________________________________________________;
(3)____________________________________________________。
在题后横线上简要说明下列操作可能造成的不良后果。
(1)滴管取用试剂后平放或倒置:__________________________。
(2)倾倒细口瓶里的药液时,标签没向着手心:__________________________。
(3)用试管刷刷洗试管时,用力过猛:__________________________。
(4)实验剩余的药品放回原瓶:__________________________。
如下图所示,把下列实验所用的主要仪器的序号和名称填在横线上:
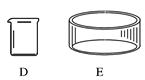
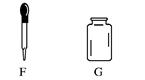
(1)吸取和滴加少量的液体需要用____________;
(2)少量溶液相互反应时,需要用____________;
(3)蒸发溶液时,需要用____________;
(4)配制溶液,溶解一定量的溶质时,需要用____________。
下表是空气中的气体成分和人体呼出的气体成分含量对照表:
| 气体成分 |
氮气 |
氧气 |
二氧 化碳 |
水 |
其他 气体 |
| 空气中的气体/% |
78 |
21 |
0.03 |
0.07 |
0.9 |
| 呼出的气体/% |
78 |
16 |
4 |
1.1 |
0.9 |
某校研究性学习小组的同学设计了简单的实验方案,验证呼出的气体与吸入空气成分的含量的不同,其主要操作步骤如下图所示。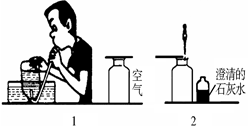
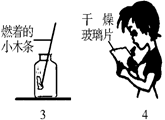
请依据图示将主要实验操作步骤及验证依据填入下表中:
| 实验步骤 |
验证依据 |
| (1)___________________________________ |
— |
| (2)___________________________________ |
根据________________________判断CO2含量不同 |
| (3)___________________________________ |
根据________________________判断O2含量不同 |
| (4)___________________________________ |
根据________________________判断含水量不同 |
石灰水可与二氧化碳反应,生成碳酸钙,碳酸钙是白色沉淀。氧气可以支持燃烧,而二氧化碳可用于灭火。在实验室中有两瓶无色气体,分别是氧气和二氧化碳,有多种方法可将它们区分开来。请你设计两种实验方法来进行鉴别。
(1)________________________________________________________________________。
(2)________________________________________________________________________。