某化学兴趣小组学习酸、碱、盐性质后,通过实验对碱的化学性质进行验证和总结,如图所示(已知:CaCl2溶液呈中性,CaCl2+Na2CO3=CaCO3↓+2NaCl).
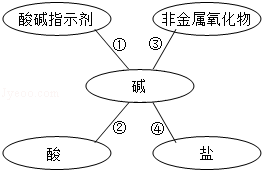
(1)甲同学将酚酞试液滴入Ca(OH)2溶液中,观察到溶液变红,得出结论:Ca(OH)2溶液呈 (填“酸性”、“碱性”或“中性”);
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到红色褪去,此时所得溶液中含有的溶质
有 (酸碱指示剂除外);
(3)丙同学根据反应③得出结论:实验室存放碱溶液时需 ;
(4)丁同学将Na2CO3溶液加入Ca(OH)2溶液中,充分反应后,与乙同学所得溶液混合,静置后发现:上层为无色透明的溶液,底部有白色沉淀.则上层溶液中一定含有的溶质是 (酸碱指示剂除外),可能含有的溶质是 ;为验证可能含有的溶质,应该补充的实验操作是 .
小柯探究pH对唾液淀粉酶活性的影响,其实验过程及结果如下:
|
组别 |
A |
B |
C |
|
试管中依次 加入物质 |
1ml唾液 |
1ml唾液 |
1ml唾液 |
|
1ml盐酸溶液 |
1ml蒸馏水 |
1ml氢氧化钠溶液 |
|
|
2ml淀粉溶液 |
2ml淀粉溶液 |
2ml淀粉溶液 |
|
|
水浴10分钟 |
37℃ |
37℃ |
37℃ |
|
各滴入2滴 碘液后的现象 |
变蓝 |
不变蓝 |
不变蓝 |
(1)B组实验不变蓝的原因是 .小柯观察到C组也不变蓝,认为氢氧化钠对酶的活性没有影响.老师提示他:"氢氧化钠会影响酶的活性."那么,是什么原因导致C组没变蓝?小柯进一步分析并做出猜想.
猜想一:氢氧化钠变质.
猜想二:氢氧化钠与碘发生了化学反应.
…
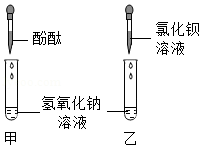
(2)小柯按图甲实验,看到溶液变红,认为氢氧化钠没有变质.小常认为他的结论是错误的,理由是 .
在小常的建议下,小柯按乙实验,溶液中没有沉淀产生,从而排除了猜想一.
(3)在原来C组实验基础上,只要继续 (写出操作和现象),就可以证明猜想二正确.
整理实验器材时,小柯将还在反应的锌和稀硫酸的残留物,倒入有少量硫酸铜溶液的废液缸中,观察到锌粒表面产生气泡的速度大大加快。对此,他十分好奇:与硫酸铜溶液混合怎么会加快锌和稀硫酸的反应速度?
查阅资料:①相互接触的两种活动性不同的金属,同时放入酸中,活动性较强的金属与酸反应产生氢气的速度会大大加快。 ②硫酸铜对锌和稀硫酸反应没有催化作用。
小柯根据下表进行实验,观察并记录现象。
|
组别 |
第一组 |
第二组 |
||
|
A |
B |
C |
D |
|
|
金属 |
锌片 |
绑有铜片的锌片 |
铁片 |
绑有铜片的铁片 |
|
30%硫酸溶液(ml) |
20 |
? |
20 |
20 |
|
产生气泡快慢 |
快 |
明显加快 |
慢 |
明显加快 |
(1)第一组实验中"?"处的数据应为 。
(2)为了定量比较产生气体的快慢,可以测量"收集相同体积的氢气所需的时间"或测量 ,然后进行比较。
(3)请推测与废液缸中少量硫酸铜溶液混合后,锌料与稀硫酸反应速度加快的原因 。
碱式氯化镁[Mg(OH)Cl]受热能分解,它分解后产物是什么?小科进行了探究。
【猜想】Mg(OH)Cl分解后产物可能有:Mg、MgCl 2、MgO、HCl气体、H 2O、Cl 2。
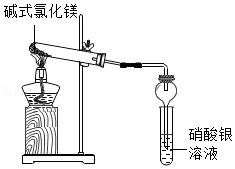
【实验一】取少量的Mg(OH)Cl放入大试管中,按如图所示装置进行实验,加热过程中观察到足量硝酸银溶液中有白色沉淀产生,一段时间后,沉淀不再产生,大试管口也没有液滴形成,管内有固体剩余,无其他现象。由此推知Mg(OH)Cl分解后产物中有 气体,无其他气体。
【实验二】取少量实验一的剩余固体于试管中,加入足量稀盐酸,没有气泡产生,由此推知Mg(OH)Cl分解后产物中没有 。
【实验三】再取少量实验一的剩余固体,加入足量稀硝酸,固体全部溶解,再滴入AgNO 3溶液,无沉淀产生,由此推知Mg(OH)Cl分解后产物中没有 。
【结论】Mg(OH)Cl受热分解的化学反应方程式为 。
小峰和小刚阅读试剂标签后发现,市场销售的高锰酸钾晶体纯度高达99.5%,含水量可以忽略不计,为探究“试管放置方式对高锰酸钾制取氧气速度和体积的影响”,他俩设计了制取氧气的直立型装置(如图),并与斜卧型装置比较,在气密性良好的装置中分别加入5.0克高锰酸钾晶体,用同一酒精灯 分别加热,用同一型号的集气瓶收集气体,每组实验进行五次,实验数据取平均值后记录如下表:
|
装置类型 |
直立型 |
斜卧型 |
|
收集1瓶氧气所需时间/秒 |
59 |
68 |
|
收集2瓶氧气所需时间/秒 |
95 |
108 |
|
收集氧气的总体积/毫升 |
525 |
476 |
(1)收集2瓶氧气,所需时间较短的装置类型是 ;
(2)等质量的高锰酸钾加热到不再产生气体,斜卧型装置收集到氧气的总体积比直立型少的原因是 ;
(3)根据2KMnO4 K2MnO4+MnO2+O2↑,算出5.0克高锰酸钾生成的氧气体积为理论值。实验中发现,斜卧型发生装置收集到的氧气体积明显大于理论值,他们对其原因进行了探究:
K2MnO4+MnO2+O2↑,算出5.0克高锰酸钾生成的氧气体积为理论值。实验中发现,斜卧型发生装置收集到的氧气体积明显大于理论值,他们对其原因进行了探究:
【提出假设】
小峰假设:反应生成的二氧化锰在较高温度下受热分解出氧气;
你的假设: 。
【设计实验】要验证小峰的假设能否成立,请设计简明的实验方案 。

海尔蒙特、普利斯特利、萨克斯等多位科学家用了几百年的时间,经过无数次的实验才对光合作用有了比较清楚地认识,有许多关于"验证叶片在光合作用和呼吸作用过程中有气体的产生和消耗"的经典实验流传至今,现将其中一个实验的思路及过程简述如下:
(注:NaHCO 3稀溶液能维持溶液中CO 2浓度恒定.其原理是当CO 2浓度降低时,NaHCO 3稀溶液能释放CO 2,当CO 2浓度升高时,NaHCO 3稀溶液能吸收CO 2.)
①剪取一烟草叶片,立即将其放入盛有NaHCO 3稀溶液的容器中,发现叶片浮于液面;
②用真空泵抽去该叶片中的气体后,发现叶片下沉至容器底部;
③将该容器放在阳光下一段时间,发现叶片逐渐上浮
④再将该容器放在黑暗环境中一段时间,发现叶片又慢慢下沉至容器底部.
请你用所学的知识对以上③、④中叶片的上浮与下沉现象进行解释. 