用Ba(OH)2溶液测定某种氮肥中(NH4)2SO4的质量分数(杂质溶于水,但不参加反应)。
实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入Ba(OH)2溶液,生成
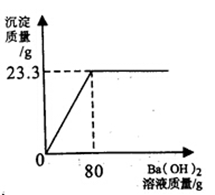
气体及沉淀质量与加入Ba(OH)2溶液的质量关系如下所示:
| 实验次序 |
1 |
2 |
3 |
| 滴入Ba(OH)2溶液的质量/g |
20 |
40 |
60 |
| 生成气体的质量/g |
0.85 |
m |
2.55 |
试分析并计算:[已知:(NH4)2SO4+Ba(OH)2=BaSO4↓+2H2O+2NH3↑]
(1)表格中m的值为 g。
(2)实验所用氢氧化钡溶液中溶质的质量分数。
(3)该氮肥中(NH4)2SO4的质量分数。(计算结果精确至0.1%)
为测定某黄铜样品中锌的含量,某同学称取20g黄铜(铜和锌的合金)样品于烧杯中,向其中加入稀硫酸至不再产生气泡为止,共消耗100g质量分数为9.8%的稀硫酸,请计算:
(1)该黄铜样品中锌的质量。
(2)反应后所得溶液的溶质质量分数(计算结果保留0.1%)。
如图是某品牌补铁剂的标签。请回答:
(1)富马酸亚铁颗粒中的铁属于元素(填“常量”或“微量”);
(2)富马酸亚铁中C、H元素的质量比为;
(3)已知富马酸亚铁(C4H2FeO4)中铁元素的质量分数为33%,若每次服用1包该补铁剂,摄入铁元素的质量为mg。
配制50g溶质的质量分数为4%的氢氧化钠溶液,需要氢氧化钠和水各多少克?若要完全中和这些溶液.需要溶质的质量分数为3.65%的稀盐酸多少克?
将铁粉和铜粉混合物7.0
,加入到盛有60.0
稀盐酸的烧杯中,恰好完全反应。此时烧杯内各物质的总质量为66.8
。试计算:
(1)原混合物中铁粉的质量分数。(精确到0.1%)
(2)反应后所得溶液中溶质的质量分数。(精确到0.1%)
将2.34
固体溶于103.4
水中得到不饱和溶液,再向所得溶液中小心滴入200
溶液。实验过程中,生成的
的质量与滴入的
溶液的质量关系如下图所示(提示:
)。
(1)计算A点处生成
的质量?
(2)计算B点溶液中
的溶质质量分数?
(若最后结果不能整除,保留小数点后一位)