(14分)据图回答下列问题:

Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是 负极反应式为:_______。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________(填Mg或Al),总反应化学方程式为___________。
Ⅱ、由Al、Cu、浓硝酸组成原电池,其正极的电极反应式为_________。
Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。

①该电池工作时,b口通入的物质为_______,c口通入的物质为______。
②该电池负极的电极反应式为:_______
③工作一段时间后,当12.8 g甲醇完全反应生成CO2时,______________NA个电子转移。
某烃A分子式是C1 398H1 278,它由4种基团组成,这4种基团分别是 (3价)
(3价) (2价);
(2价); (2价);(CH3)3C—(1价)
(2价);(CH3)3C—(1价)
已知,该分子结构中没有苯环连接苯环、炔键连接炔键的情况,试求A分子中含有这4种基团各几个?
在沥青中存在一系列结构相似的稠环芳香烃。这一系列化合物中的前三个同系物的结构简式如右图所示。
(1)萘的分子式是______________,芘的分子式是______________,蒽并蒽的分子式是______________。
(2)上述一系列化合物中,相邻两化合物分子式之差为CnHm,则n值为______________,m值为______________。
(3)这一系列有机物的通式可用含x的代数式来表示(x为自然数1,2,3,4…),则该通式为______________。
(4)随着x值的增大,这一系列化合物含碳的质量分数的极限数值为______________。
矿物能源是现代人类社会赖以生存的重要物质基础。目前世界矿物能源仍以化石燃料煤、石油、天然气为主。
(1)试以C、CnH2n+2、CH4为代表,写出其完全燃烧的化学方程式:
_____________________、_____________________、_____________________。
等质量的上述三种燃料完全燃烧,对环境的负面影响最小的是_____________________。
(2)化石燃料储存的能量来自绿色植物吸收的太阳能,光合作用把太阳能转化成___________能,生成糖(以葡萄糖C6H12O6为代表),则光合作用的总反应式为_____________________。
(3)光合作用释放的O2来自于参加反应的哪种物质?
现有饱和一元醇的混合物和饱和一元羧酸的混合物在一定条件下反应生成多种酯的混合物,酯的相对分子质量分别为M1、M2、M3,并依次增加14。经分析,相对分子质量为M2的酯,其中氧元素所占的质量分数为31.4%,并有三种酯的同分异构体。
请完成下列问题:
(1)相对分子质量为M2的酯的分子式为______________________________。
(2)饱和一元羧酸的分子式分别为______________________,______________________。
(3)参加反应的醇的结构简式为_______________、_______________、_______________、_______________(不必填满)。
(4)与相对分子质量为M1的酯互为同分异构体,能发生银镜反应,能与金属钠反应产生氢气的有机物的同分异构体有_______________种。
我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。这一材料是由江苏华信塑业发展有限公司最新研发成功的新材料,并成为公安部定点产地。PETG的结构简式为: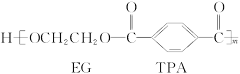
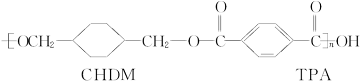
已知:
②RCOOR1+R2OH RCOOR2+R1OH(R、R1、R2表示烃基)
RCOOR2+R1OH(R、R1、R2表示烃基)
这种材料可采用下列合成路线: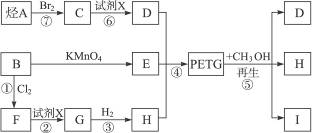
试完成下列问题:
(1)反应②⑥加入的试剂X是___________。
(2)⑤的反应类型是___________。
(3)写出结构简式:B___________,I___________。
(4)合成时应控制的单体的物质的量
n(D)∶n(E)∶n(H)= ___________∶___________∶___________。(用m、n表示)
(5)写出化学反应方程式:
反应③:_______________________________________________________;
反应⑥:_______________________________________________________。