在复习元素周期律过程中,某研究性学习小组的几位同学拟通过具体的实验来探讨某些金属元素的性质差异,下面是他们设计的探究性实验方案,请填写下列空白:
(1)实验目的:比较钠、镁、铝金属性强弱。
(2)实验用品:酒精灯、 、试管、试管夹、砂纸、滤纸;钠、镁条、铝片、酚酞、蒸馏水、6 mol·L-1的盐酸
(3)实验过程与现象记录
Ⅰ.甲同学的方案如下:
| 实验过程 |
预期现象 |
实际观察到的现象 |
| a取已切去表皮的一小块金属钠,放入盛有水的某容器中 |
立即剧烈反应 |
开始时钠块浮在水面上不反应,稍后才开始与水剧烈反应 |
| b向盛有适量水(内含2滴 酚酞的试管中加入一小段镁条 |
有气泡产生,溶液变红色 |
没有相应现象,加热后仍无明显变化 |
| c向两支盛有3mL6mol·L-1盐酸的试管中加入大小相同的镁片和铝片 |
镁、铝与盐酸反应产生气泡剧烈程度不同 |
镁与盐酸反应产生气泡速率较快 |
①你认为a、b两步实验中出现异常现象的可能原因是:
a
b
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为
Ⅱ乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作
是
(共12分)某同学利用以下装置制备氨气并探究氨气的还原性。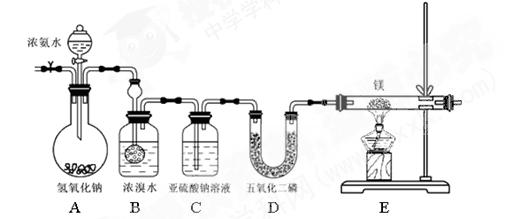
实验步骤及现象:①连接仪器并检验装置气密性②通入惰性气体(不与镁反应),排出装置中的空气③打开分液漏斗活塞,观察到B中浓溴水颜色变浅至褪色,C中产生无色气泡④点燃酒精灯,观察E中固体变成了黄绿色。
查阅资料:氮化镁是黄绿色固体,遇水剧烈反应生成两种碱。
请回答下列问题:
(1)A中氢氧化钠的作用为(用简要的语言和方程式来说明)
(2)写出B处反应的化学方程式
(3)亚硫酸钠的作用
(4)此装置有不足之处,请说明
(5)某同学要继续探究E中固体成分。将E中的固体放入稀盐酸中,观察到固体溶解并产生气泡,写出此过程中反应的化学方程式
Ⅰ.如图所示为常见仪器的部分结构。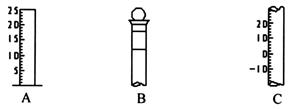
(1)请写出下列仪器的名称:A,B,C。
(2)仪器B上标记有(填序号)。
①质量②温度③刻度线④浓度⑤容积
(3)仪器B使用前必须。
Ⅱ.现用98%的浓H2SO4(密度为1.84g/cm3)来配制480mL0.2mol/L的稀H2SO4。
有关操作为:①计算所需浓硫酸的体积②量取一定体积的浓硫酸③稀释、冷却④转移、洗涤⑤定容⑥摇匀
回答下列问题
(4)应量取的浓硫酸体积是,实验中所用的玻璃仪器除烧杯、玻璃棒、
量筒、胶头滴管外还有;
(5)第③步中稀释浓硫酸的操作是
(6)将所配制的稀H2SO4进行测定,发现实际浓度大于0.2mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母)。
| A.用量筒量取浓硫酸时,仰视量筒的刻度 |
| B.容量瓶未干燥即用来配制溶液 |
| C.浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容 |
| D.往容量瓶转移时,有少量液体溅出 |
E.烧杯未进行洗涤
F.在容量瓶中定容时俯视容量瓶刻度线
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
、某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数 。
。
请回答:(1)以上步骤有错误的是(填编号),
该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”) ______;
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无响”)____________;
(3)判断滴定终点的现象是:锥形瓶中溶液从色变为色,且半分钟不变色;
(4)右图是某次滴定时的滴定管中的液面,其读数为mL;
(5)根据下列数据:请计算待测盐酸溶液的浓度:mol/L。
| 滴定次数 |
待测体积(ml) |
标准烧碱体积(ml) |
|
| 滴定前读数 |
滴 定后读数 定后读数 |
||
| 第一次 |
20.00 |
0.40 |
20.40 |
| 第二次 |
20.00 |
4.00 |
24.00 |
| 第三次 |
20.00 |
2.00 |
24.10 |
亚硝酸钠属剧毒物质,是一种食品护色剂。人体摄入过多的亚硝酸钠,30min即出现恶心、呕吐、全身 无力、皮肤青紫等中毒症状,严重者昏迷、抽搐、呼吸衰竭而死亡。我国因亚硝酸钠严重污染或以“工业盐”(亚硝酸钠)作为食盐误食引起恶性食物中毒事故屡有发生。所以 ,在肉制品加工中使用护色剂必须严格控制其使用量,确保食用安全。
(1) 已知NaNO2能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O,反应中氧化剂是_________,若有2mol NaNO2发生反应转移电子的物质的量_________mol。
(2)根据上述反应,可以用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有①自来水②碘化钾淀粉试纸③淀粉④白糖⑤食醋⑥白酒。进行实验时,必须选用的物质有_____________。
(3)若误食亚硝酸盐会导致血红蛋白中亚铁离子转化为铁离子而中毒。服用维生素C可解除亚硝酸盐中毒。下列叙述正确的是_________。
| A.亚硝酸盐是还原剂 | B.维生素C是还原剂 |
| C.维生素C能把亚铁离子氧化为三价铁离子 | D.亚硝酸盐被氧化 |
下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明。请根据此表,结合化学和生物学科的知识,回答下列问题。
配料表 |
精制海盐、碘酸钾 |
| 含碘量 |
20~40mg/kg |
| 卫生许可证号 |
××卫碘字(1999)第001号 |
| 分装日期 |
见封底 |
| 储藏方法 |
密封、避光、防潮 |
| 食用方法 |
烹调时,待食品熟后加入碘盐 |
(1)要在食盐中加碘,是因为碘是人体内合成____________激素的主要原料,缺碘会引起疾病。
(2)食盐中加碘,这碘指的是(填
 化学式),其中碘元素的化合价为__________。
化学式),其中碘元素的化合价为__________。
(3)根据含碘盐的食用方法,可推测碘酸钾在受热时容易___________________。