某化学兴趣小组用如图所示装置研究以下两个问题。
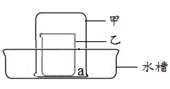
【实验1】可燃物燃烧的条件
步骤1:水槽中放有一定量热水,水面下a处放一小块白磷,此时观察到白磷不燃烧。
步骤2:在乙中放入二氧化锰和过氧化氢溶液,立即将甲倒扣在乙上。
此时观察到甲中水面下降,白磷露出水面, 。
此实验运用对比的方法研究了可燃物燃烧的一个条件是 。
【实验2】浓盐酸的性质
步骤1:a处放一湿润的紫色石蕊试纸,乙中放入浓盐酸,立即将甲倒扣在乙上。此时观察到试纸变为红色。说明浓盐酸具有的性质为 。
步骤2:将试纸取出,立即向水槽中加入滴有酚酞的氢氧化钠溶液,此时观察到红色溶液逐渐变为无色。出现此现象的原因是 。
某校化学兴趣小组进行粗盐(含有泥沙)提纯实验,并利用所得精盐配制100g20%的氯化钠溶液。
实验一:如图1是甲同学进行粗盐提纯实验的操作示意图。

(1)操作①中的一处明显错误是 。
(2)操作⑤对应的实验中,停止加热的恰当时机是 。
(3)该同学实验中缺少过滤操作,在此操作中玻璃棒的作用是 。
实验二:乙同学用提纯得到的精盐配制100g20%的氯化钠溶液。
(4)配制时,除如图1提供的仪器外,还需要试剂瓶、镊子和 (填一种仪器名称)。
(5)若其他操作均正确,采用如图2所示观察方式量取水,则所配溶液的溶质质量分数 _ (填">"、"<"或"=")20%。
实验室制取某些气体所用的装置如图所示,请回答:

(1)图中标号a的仪器名称是 .
(2)实验室用高锰酸钾制取氧气,反应的化学方程式是 .若用D装置收集氧气,气体应从 (填"b"或"c")端进入.
(3)乙炔(C 2H 2)是一种可燃性气体,已知实验室可用块状电石和水在常温下反应制取,该反应非常剧烈,则制取乙炔气体的发生装置最好选择 (填字母).
(4)F是某同学刚收集的一瓶二氧化碳气体,请设计实验进行检验 (写出具体实验操作和现象).
利用如图1装置,小卫设计并实施了下列实验,(压强传感器用于测量抽滤瓶内压强变化:各数据均于同温下测定获得)

实验Ⅰ:再小试管中加入8mL溶质质量分数为3%的双氧水(ρ=1g/mL),在抽滤瓶中分别加入不同质量的MnO 2,使其反应并启动传感器,记录容器内压强变化于图2中。
实验Ⅱ:在抽滤瓶中加入0.1g MnO 2,在小试管中分别加入不同体积溶质质量分数为3%的双氧水,使其反应并启动传感器,记录容器内压强变化于图3中。
请根据以上实验回答下列问题:
(1)使容器内压强增大的反应的化学方程式: 。
(2)根据图2可发现,该实验条件下,30s内催化分解8mL溶质质量分数为3%的双氧水,MnO 2的最小用量为 g;
(3)根据图3可发现,0.1g MnO 2至少能快速催化分解 g过氧化氢;
(4)根据图2与图3可发现,MnO 2的用量总体上与O 2产量 (填"正相关"、"不相关"或"负相关"),根据图3还可发现,该试验中,O 2产量总体上与双氧水用量是 (填"正比"或"反比");
(5)下列因素中,与本实验所测数据的精确度有关的是
| A. |
反应容器的气密性 |
| B. |
称量MnO 2质量的精准度 |
| C. |
量取双氧水体积的精准度。 |
DIY冰淇淋,配料:奶油、鲜牛奶、蔗糖、生鸡蛋、香兰素(分子式为C 8H 8O 3)。将上述配料加入金属容器中,搅拌均匀,再向容器中加入适量液氮,继续搅拌至均匀无结块时,美味的冰淇淋就可以品尝了。
(1)鸡蛋蛋清中含有的营养物质主要是 ;向蛋清浓溶液中滴加饱和硫酸铵溶液,可以观察到有 生成;
(2)每个香兰素分子由 个原子构成,其中碳元素的质量分数为 %(保留一位小数);
(3)美味冰淇淋的制作秘诀在于速冻,此过程中,液氮变成氮气,该变化属于 变化(填"物理"或"化学");
(4)若制作时没液氮,也可使用 代替。
莫凡同学完成镁与稀盐酸反应的实验后,观察到有灰白色沉淀生成的"异常"现象,引起了他的兴趣,并进行了以下探究。
【初步探究】出现灰白色沉淀是否为偶然现象。
【实验Ⅰ】向4份相同体积与浓度的稀盐酸中分别加入一定长度的某种镁带,现象如下:
|
实验组别 |
A |
B |
C |
D |
|
镁带长度 |
1cm |
2cm |
3cm |
4cm |
|
沉淀量 |
无沉淀生成 |
少量沉淀 |
沉淀较多 |
沉淀很多 |
【实验结论】并非偶然,据表分析, 是实验出现"异常"的主要因素。
【再次探究】该沉淀的成分
【猜想假设】猜想1:Mg;猜想2:MgCl 2
【实验Ⅱ】
|
序号 |
实验操作 |
实验现象 |
实验结论 |
|
① |
取1g样品,加入足量 ,振荡 |
未见气泡 |
猜想1错误 |
|
② |
取1g样品,加入5mL蒸馏水,振荡 |
沉淀未溶解 |
猜想2错误 |
|
③ |
取1g MgCl 2固体,加5mL蒸馏水,振荡 |
固体全部溶解 |
【交流讨论】
(1)莫凡同学做出猜想Ⅰ的依据是他认为反应物Mg过量,作出猜想2的依据是他认为生成物MgCl 2 。
(2)从实验设计的角度讲,实验③的作用是 。
【深入探究】该沉淀的物质组成
【查阅资料】
灰白色沉淀的成分为碱式氯化镁,它存在多种组成,化学式可表示为Mg x(OH) yCl z•nH 2O[即每份Mg x(OH) yCl z结合了n份H 2O],它受热分解可产生氧化镁、氯化氢和水。
【实验Ⅲ】
洗去沉淀表面杂质并室温晾干,取其7.07g,用如图装置(夹持仪器未画出)按照正确的操作步骤进行实验,待反应停止后,测得硬质玻璃管中剩余固体质量为4.00g,装置B的质量增加了2.34g。
【问题讨论】
(1)反应停止后,应继续通入N 2一段时间,目的是 。
(2)该沉淀中,镁、氯的离子个数比n(Mg 2+):n(Cl ﹣)= 。
(3)若沉淀Mg x(OH) yCl z•nH 2O中,n=5,则X、Y、Z的数值依次为 。
