甲、乙两同学在学完酸的化学性质后,做了如下实验:

【观察与讨论1】甲同学在做实验时观察到的明显现象是 ① 。再滴加无色酚酞溶液,无明显现象(已知CaCl2溶液呈中性)。
【观察与讨论2】乙同学在做实验时开始没有观察到气泡产生,于是对碳酸钠能否与盐酸反应表示怀疑。甲同学通过查阅资料得知:在碳酸钠溶液中滴加少量稀盐酸,先发生反应Na2CO3+HCl=NaCl+NaHCO3,继续滴加稀盐酸,再发生反应NaHCO3+HCl=NaCl+H2O+CO2↑。所以甲同学认为,乙同学实验时还应 ② ,才能观察到有气泡产生。
【观察与讨论3】甲同学先将废液缓慢倒入一洁净的废液杯中,乙同学在观察到气泡产生后,也将实验废液缓慢倒入该废液杯中,没有观察到明显现象。经过讨论确定,甲同学的试管中废液含有的溶质一定有 ③ ,乙同学的试管中废液含有的溶质一定有 ④ (均写化学式)。
为了处理实验后产生的废液,甲、乙同学决定对废液杯中最终废液溶质的成分进行探究。
【提出问题】最终废液中含有什么溶质?
【猜想与假设】猜想1:废液中含有 (写化学式)两种溶质。
猜想2:废液中含有 (写化学式)三种溶质。
猜想3:废液中含有NaHCO3、CaCl2、 NaCl三种溶质。
【活动与探究】甲、乙同学为了验证猜想,进行了如下实验:
甲同学实验:取少量废液于试管中,向其中滴加盐酸,无气泡产生。
乙同学实验:取少量废液于试管中,向其中滴加紫色石蕊试液,溶液变红色。
【结论与反思】(1)猜想 (填“1”或“2” 或“3”)正确。
(2)要得到相同的结论,还可采用很多种方法。如加入氧化铁粉末,可观察到溶液呈 色,该反应的化学方程式为 。
【表达与交流】甲、乙同学确认了最终废液中溶质的成分,若直接排放,可能造成的危害是 ,你认为处理该废液的方法是 。
铜是人类认识并应用最早的金属之一,我国有着使用铜器的悠久历史。
(1)5G基站供电系统多用铜作导线,是因为铜具有良好的 性和延展性;
(2)宋代《梦溪笔谈》记载“熬胆矾铁釜久之亦化为铜”叙述的是硫酸铜溶液和铁反应生成铜,说明铁的金属活动性比铜 ;
(3)木炭可以与氧化铜反应,化学方程式为C+2CuO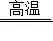 2Cu+CO2↑,该反应中CuO发生了 (选填“氧化”或“还原”)反应。
2Cu+CO2↑,该反应中CuO发生了 (选填“氧化”或“还原”)反应。
化学是一门以实验为基础的科学,对比法是一种常见的实验方法,回答下列问题:
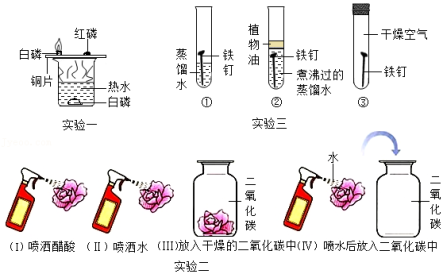
(1)实验一说明可燃物燃烧需要温度达到着火点的现象是 ;
(2)实验二喷水后的石蕊纸花放入二氧化碳中,纸花由紫色变为 色;
(3)实验三说明铁生锈是铁与氧气、 共同作用的结果。
O2是人类生活不可缺少的物质,制取O2的方法很多。请回答下列问题:
(1)KMnO4分解法:该反应的化学方程式为 ;
(2)KClO3分解法:应选用图中的 (填图中装置对应的字母)作发生装置;
(3)H2O2分解法:常温下H2O2分解缓慢,通常加入少量MnO2,则MnO2的作用为 ;
(4)可以用C所示装置来收集O2,体现了O2 的性质;
(5)已知N2的沸点为﹣196℃,O2的沸点为﹣183℃。工业上在低温下加压,先使空气液化,然后蒸发,则O2为 (填“先”或“后”)蒸发出来的气体。

下列装置常用于实验室制取气体,请回答下列问题。
(1)写出仪器①的名称 。
(2)实验室用加热高锰酸钾的方法制取氧气,应选择的发生装置是 (填字母代号),在装入药品前应先检查装置的 。
(3)用装置C收集氧气时,其验满的方法是 。
某同学做氧气的性质实验,如图为木炭在氧气中燃烧的实验示意图。
实验步骤:
①用排水法收集好一瓶氧气。
②……
③用坩埚钳夹取一小块木炭,在酒精灯上加热到发红,插入到盛满氧气的集气瓶中,燃烧停止后,取出坩埚钳。
④向集气瓶中加入少量澄清石灰水,振荡。
根据实验操作,通过分析,回答下列问题:
(1)步骤②具体操作为 。
(2)步骤③操作中,最好是将烧红的木炭由瓶口缓慢插入到盛满氧气的集气瓶中,这一实验操作的主要目的是 。
(3)步骤④操作中,可观察到澄清石灰水变浑浊,其发生反应的化学方程式为 。
(4)酒精(化学式C 2H 5OH)和木炭都是常用的燃料,若取相同质量的C 2H 5OH和C在氧气中完全燃烧,两者中消耗O 2的质量较少的是 (填"C 2H 5OH"或"C")。
