【改编】(15分)过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素,反应的化学方程式为:
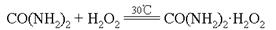 。过氧化尿素的部分性质如下:
。过氧化尿素的部分性质如下:
| 分子式 |
外观 |
热分解温度 |
熔点 |
溶解性 |
| CO(NH2)2·H2O2 |
白色固体 |
45℃ |
75~85℃ |
易溶于水、有机溶剂 |
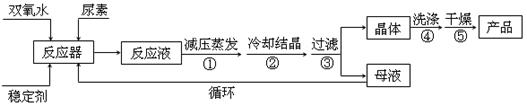
合成过氧尿素的流程及反应装置图如下:
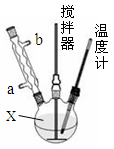
请回答下列问题:
(1)仪器X的名称是 ,冷凝管中冷却水从 (填“a”或“b”)口进入;
(2)反应器的加热方式是 ;
(3)搅拌器是否可用铁质材料 (填“是”或“否”),原因是 ;
(4)步聚①采用减压蒸发的原因是 ;
(5)下列选项中最适合作为步聚④的洗涤液是 ;
a.冰水
b.热水
c.饱和NaCl溶液
d.酒精和水的混合液
(6)准确称取0.5000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol·L-1 H2SO4,用0.1000 mol·L-1 KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应),则产品中过氧化尿素的质量分数为 ;若滴定前滴定管尖嘴处有气泡,滴定后消失,则测得的过氧化尿素含量 (填“偏高”、“偏低”或“不变”)。
石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。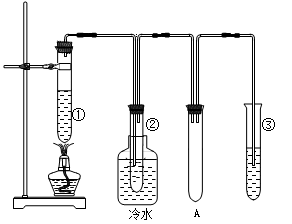
实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现象回答下列问题:
(1) 装置A的作用是______________________________
(2) 试管①中发生的主要反应有:
C17H36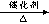 C8H18+C9H18 C8H18
C8H18+C9H18 C8H18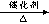 C4H10+C4H8
C4H10+C4H8
丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为_____________和________________,这两种有机物混合后在一定条件下可聚合成高分子化合物,其反应类型属于________反应。其可能结构为( )(答案可能不止一个,下同)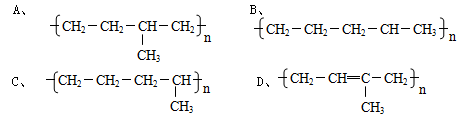
(3)写出试管③中反应的一个化学方程式_____________________________,该反应的类型为__________反应。
(4)试管②中的少量液体的组成是____________(填序号)
①甲烷②乙烯③液态烷烃④液态烯烃
某化学兴趣小组为了测定某铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请据此项回答相应问题。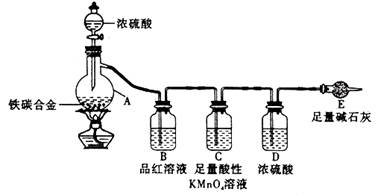
Ⅰ探究浓硫酸的某些性质
(1)按图示连接装置,检查装置的气密性,称量E的质量。
(2)将a g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为____________,
未点燃酒精灯前,A、B均无明显现象,其原因是:_______。
(3)点燃酒精灯一段时间后,A、B中可观察到明显现象。
A中开始发生反应的化学方程式为:2Fe +6H2SO4 Fe2(SO4)3 + 3SO2↑ +6H2O
Fe2(SO4)3 + 3SO2↑ +6H2O
和______________________________________ (写化学方程式)。
B中的现象是_________,由此可得到浓硫酸具有_______性,C装置的作用。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式__ __。
(5)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是_____________________________________。
Ⅱ测定铁的质量分数
(6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。
铁碳合金中铁的质量分数为_____________________(写表达式),为使实验数据更为精确,可在装有碱石灰的干燥管后加入________________________________。
(一)在配制物体的量浓度溶液时,下列操作出现的后果是(填: “偏低”、“偏高”、“无影响”):
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体。
(2)配制氯化钠溶液时,容量瓶中有少量水。。
(3)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线。。
(二)实验室常用标准NaOH溶液测定未知盐酸溶液的浓度。
(1)配制0.5mol·L-1NaOH溶液250mL所需的玻璃仪器为。
(2)用滴定管准确量取20.00毫升未知浓度盐酸于锥形瓶中,加入酚酞作指示剂,用NaOH溶液滴定到终点。
某学生进行了三次实验,实验数据如下表:
| 实验编号 |
盐酸体积( mL ) |
标准NaOH溶液的体积(mL) |
| 1 |
20.00 |
18.20 |
| 2 |
17.10 |
|
| 3 |
16.90 |
滴定中误差较大的是第_____次实验,造成这种误差的可能原因是_______________。
A.滴定管在装标准NaOH溶液前未润洗
B.滴定开始前装标准NaOH溶液滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
C.滴定开始前装标准NaOH溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.在装未知浓度盐酸前锥形瓶里面有少量水,未烘干
E.达到滴定终点时,俯视溶液凹液面最低点读数
F.滴定过程中,锥形瓶摇荡得太剧烈,以至有些液滴飞溅出来
G.滴定到终点时,溶液颜色由无色变到了红色
(3)该同学所测得盐酸溶液的物质的量浓度为___________(结果保留三位小数)。
实验室常用加热铵盐和碱的固体混合物的方法制取氨气。
根据下图回答问题: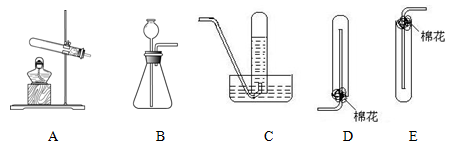
(1)实验室制取氨气的发生装置为(填序号),该反应的化学方程式为。
(2)下列气体可以用与氨气相同的收集装置收集的是(填序号)。
A. H2 B. CO2
氯气是一种化学性质活泼的气体。
⑴氯气是一种具有气味的气体,密度比空气的(填“大”或“小”),若采用图中装置收集氯气,则氯气应由管(填“A”或“B”)通入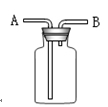
⑵氯气与NaOH溶液反应的化学方程式为,该反应可用于工业上制取漂白液,其有效成分是。