(共16分)近年来对CO2的有效控制及其高效利用的研究正引起全球广泛关注。据中国化工报报道,美国科学家发现了一种新的可将CO2转化为甲醇的高活性催化体系,比目前工业使用的常见催化剂快近90倍。由CO2制备甲醇过程可能涉及反应如下:
反应Ⅰ: CO2(g)+3H2(g)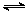 CH3OH(g) +H2O(g) △H 1=-49.58 kJ•mol-1
CH3OH(g) +H2O(g) △H 1=-49.58 kJ•mol-1
反应Ⅱ:CO2(g)+H2(g)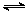 CO(g)+H2O(g) △H 2
CO(g)+H2O(g) △H 2
反应Ⅲ: CO(g)+2 H2(g)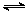 CH3OH(g) △H 3=-90.77 kJ•mol-1
CH3OH(g) △H 3=-90.77 kJ•mol-1
回答下列问题:
(1)反应Ⅱ的△H 2= ,反应Ⅲ自发进行条件是 (填“较低温”、“较高温”或“任何温度”)。
(2)在一定条件下2L恒容密闭容器中充入一定量的H2和CO2仅发生反应Ⅰ,实验测得在不同反应物起始投入量下,反应体系中CO2的平衡转化率与温度的关系曲线,如下图所示。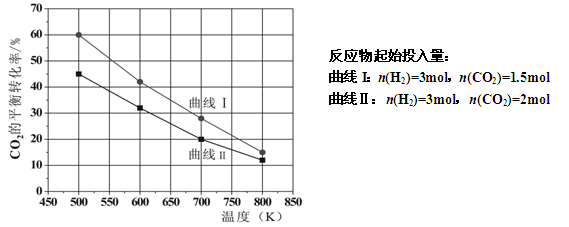
①据图可知,若要使CO2的平衡转化率大于40%,以下条件中最合适的是 ;
A.n(H2)=3mol,n(CO2)=1.5mol; 650K
B.n(H2)=3mol,n(CO2)=1.7mol;550K
C.n(H2)=3mol,n(CO2)=1.9mol; 650K
D.n(H2)=3mol,n(CO2)=2.5mol;550K
②在温度为500K的条件下,充入3mol H2和1.5mol CO2,该反应10min时达到平衡:
a.用H2表示该反应的速率为 ;
b.该温度下,反应I的平衡常数K= ;
c.在此条件下,系统中CH3OH的浓度随反应时间的变化趋势如图所示,当反应时间达到3min时,迅速将体系温度升至600K,请在图中画出3~10min内容器中CH3OH浓度的变化趋势曲线:
(3)某研究小组将一定量的H2和CO2充入恒容密闭容器中并加入合适的催化剂(发生反应I、Ⅱ、
Ⅲ),测得了不同温度下体系达到平衡时CO2的转化率(a)及CH3OH的产率(b),如图所示,请回答问题: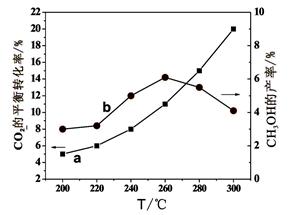
①该反应达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是 (选填编号)。
A.改用高效催化剂
B.升高温度
C.缩小容器体积
D.分离出甲醇
E.增加CO2的浓度
②据图可知当温度高于260℃后,CO的浓度随着温度的升高而 (填“增大”、“减小”、“不变”或“无法判断”),其原因是 。
工业上从海水 提取溴,涉及到“浓缩”、“氧化”、“提取”等步骤,其中在“提取”过程中,可用空气把溴吹出,然后用碳酸钠溶液吸收,这时溴转化为Br-离子和BrO3-离子,同时有二氧化碳气体生成。最后用硫酸酸化,单质溴又从溶液中析出。
提取溴,涉及到“浓缩”、“氧化”、“提取”等步骤,其中在“提取”过程中,可用空气把溴吹出,然后用碳酸钠溶液吸收,这时溴转化为Br-离子和BrO3-离子,同时有二氧化碳气体生成。最后用硫酸酸化,单质溴又从溶液中析出。
(1)写出单质溴与碳酸钠溶液反应的化学方程式________________________________。
(2)用硫酸酸化时,每转移1 mol电子,可以生成单质溴___________ mol。
(3)已知在酸性条件下有以下反应关系:
①KBrO3能将KI氧化成I2或KIO3,其本身被还原为Br2;
②Br2能将I¯氧化为I2;
③KIO3能将I¯氧化为I2,也能将Br-氧化成Br2,其本身被还原为I2。
Br2、BrO3-、I2、IO3-的氧化性由强到弱的顺序为__________________________。
(4)以下离子方程式错误的是______________(选填答案编号)。
| A.IO3-+ Br-→I-+ BrO3- |
| B.6I-+ BrO3-+ 6H + → 3I2 + Br-+ 3H2O |
C.5I-+ 6BrO3-+ 6H + →3 Br2+ 5 IO3 -+ 3H2O -+ 3H2O |
D.5I-+ 2BrO3 -+ 6H + → Br2 + IO3-+ 2I2 + 3H2O -+ 6H + → Br2 + IO3-+ 2I2 + 3H2O |
我国的探月工程正在有计划的进行着,最近发射的嫦娥二号卫星又圆满完成了多项科学任务。月球上的主要矿物有辉石[CaMgSi2O6]、斜长石[KAlSi3O8]和橄榄石(可分为铁橄榄石[Fe2SiO4]、镁橄榄石[Mg2SiO4]、铁-镁橄榄石[(Mg∙Fe)2SiO4])等。
(1)铁橄榄石中铁元素化合价为______,硅元素原子核外电子排布式为_____________。
(2)硅元素的原子核外共有______种不同能级的电子,其原子最外层共有_____种不同运动状态的电子。
(3)月球上的上述主要矿物中,属于短周期元素的原子半径由大到小依次为__________
(填相应的元素符号),在这些短周期元素中,其单质晶体微粒间存在两种相互作用的是_____元素。
(4)某元素与氧元素同周期,且与氧元素组成的化合物中氧元素显正+2价,写出一个化学方程式 ,说明该元素与氧元素的非金属性的强弱______________________
,说明该元素与氧元素的非金属性的强弱______________________ __。
__。
不同卤素原子间可以通过共用电子对,形成卤素互化物,其通式为:XX′n(n
= 1,3,5,7;且非金属性X′>X)。卤素互化物大多为强氧化剂。回答下列问题:
(1)卤素互化物中,沸点最低的应是(写分子式,下同)。
(2)若n = 7,则最可能生成的卤素互化物应为。
(3)现将23.3gBrCln溶于水,再通入过量SO2,生成HBr、HCl、H2SO4等三种酸,然后向该混 合酸溶液中加入过量Ba(NO3)2溶液后,过滤,最后向滤液中加入过量的硝酸银溶液,结果可生成77.3g沉淀,求n的值(写出计算过程)。
合酸溶液中加入过量Ba(NO3)2溶液后,过滤,最后向滤液中加入过量的硝酸银溶液,结果可生成77.3g沉淀,求n的值(写出计算过程)。
(4)某卤素互化物与水的反应为 ClFn + H2O → HClO3 + Cl2 +O2 + HF,若ClFn与H2O的物质的量之比为3∶5,求n的值(写出计算过程)。
氢氧化钡是一种广泛使用的化学试剂,现通过下列实验测定某试样中Ba(OH)2·nH2O的含量。
(1)称取3.50g试样溶于蒸馏水配成100ml溶液,从中取出10.0ml溶液于锥形瓶中,加2滴指示剂,用0.1000mol/L的标准盐酸溶液滴定至终点,共消耗标准液20.0ml(杂质不与酸反应),该试样中氢氧化钡的物质的量为____________;
(2)取5.25g试样加热至恒重(杂质受热不分解),称得质量为3.09g,求Ba(OH)2·nH2O中的n 的值(写出计算过程)
的值(写出计算过程)
分子式为C8H13O2Cl的有机物A在不同条件下能发生如下图所示的一系列转化:
(1)写出下列有机物的结构简式
A__________________,B___________________,C___________________
(2)用化学方程式表示下列反应
① A与NaOH溶液共热:___________________________________________
② F与KOH醇溶液共热:__________________________________________
③ C→G: _______________________________________________
_______________________________________________
(3)G的氧化产物与C在一定条件下反应生成环状化合物的化学方程式:
___________________________________________________________
G的氧化产物与C在一定条件下反应生成高分子化合物的结构简式_______________。