在生产生活中,卤族元素(F、Cl、Br、I)的单质及化合物用途广泛。
(1)溴元素在周期表中的位置为 。
(2)下列说法中正确的是 。
| A.CCl4和XeF2分子中各原子最外层均满足8e-结构 |
| B.Cl2O5和Cl2O7都是酸性氧化物 |
| C.氟非金属性强于氯,故氢氟酸的酸性强于盐酸 |
| D.F-、Cl-、Br-、I-等离子的还原性逐渐增强 |
(3)已知:HCl的沸点是﹣85.0℃,HF的沸点是19.5℃。HF的电子式为 ;从HF、HCl混合气体中分离出HF的方法是 。
(4)向NaClO浓溶液中加入Al2(SO4)3浓溶液,迅速生成大量白色沉淀,同时有无色气体产生。生成白色沉淀的离子方程式为 。无色气体的成分为 。
(5)潮湿的氯气与碳酸钠粉末反应可用于制取氯的最低价氧化物,反应还同时生成两种盐,该反应的化学方程式为 。
(6)已知:还原性HSO3¯>I¯,氧化性IO3¯> I2,在下图中画出向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液的过程中,析出I2的物质的量与KIO3的物质的量之间关系的曲线。

镁橄榄石主要成分是Mg2SiO4,电解法促进镁橄榄石固定CO2的工艺流程如下图所示:
已知:Mg2SiO4(s)+4HCl(aq) 2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
固碳时主要反应的方程式为NaOH(aq)+CO2(g)=NaHCO3(aq)。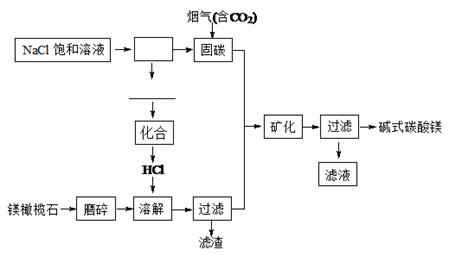
(1)上图方框里的操作名称是,横线上的物质有(填化学式)。
(2)下列物质中也可用作“固碳”的是(填字母序号)。
| A.CaCl2 | B.NH3·H2O |
| C.Na2CO3 | D.H2O |
(3)由下图可知,90 ℃后曲线A溶解效率下降,分析其原因。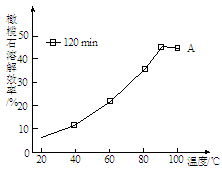
(4)经分析,所得碱式碳酸镁沉淀中含有少量NaCl。为提纯,可采取的方法是。本流程中可循环利用的物质是(填化学式)。
(5)另一种橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为。
天然气含有硫化氢气体,回收并综合利用硫化氢有重要的经济价值和环境保护意义。如硫化氢可经过一系列反应制得硫酸:
(1)物质发生不完全燃烧时的反应热难以通过实验测得。已知硫化氢气体的燃烧热是586 kJ/mol,固体硫单质的燃烧热是297kJ·mol-1。写出硫化氢气体不完全燃烧生成固体硫单质的热化学方程式。
(2)工业生产中硫化氢尾气可用NaOH溶液吸收。
①吸收尾气后得到的Na2S溶液显性(填“酸”、“碱”、“中”);
②下列与H2S、NaHS和Na2S相关的离子方程式正确的是(填字母序号)_________。
| A.H2S+OH—=HS—+H2O | B.HS—+H2O=H2S+OH— |
C.HS—+H2O S2—+H3O+ S2—+H3O+ |
D.S2—+H2O H2S+2OH— H2S+2OH— |
(3)在一定温度下,某容器中发生2H2S(g) 2H2(g)+S2(g)的反应,测得相应时间时部分物质的浓度(mol·L-1)如下表,根据表中数据回答问题:
2H2(g)+S2(g)的反应,测得相应时间时部分物质的浓度(mol·L-1)如下表,根据表中数据回答问题:
 时间 时间物质 |
0 min |
20 min |
60 min |
90 min |
120 min |
| H2S |
0.006 |
0.005 |
|||
| H2 |
0 |
0.002 |
0.004 |
||
| S2 |
0 |
0.002 |
0.0025 |
①判断90 min时反应速率v(正)______v(逆)(填“>”、“=”或“<”);
②求该温度下反应的化学平衡常数(不必写出计算过程)K=_________。
(4)以硫化氢为原料,使用质子固体电解质(能传导H+)构成燃料电池,硫化氢放电后生成硫蒸气(化学式S2),该燃料电池的负极反应式为_____________。
(5)硫酸是强酸,在图中画出硫酸溶液和氢氧化钠溶液反应过程的能量变化示意图。
苯乙醛( )主要存在于烟叶中,有浓郁的玉簪花香气,用于合成香料。现有如下转化关系,其中C能使溴的四氯化碳溶液褪色,E继续被氧化生成F,F的相对分子质量为90。
)主要存在于烟叶中,有浓郁的玉簪花香气,用于合成香料。现有如下转化关系,其中C能使溴的四氯化碳溶液褪色,E继续被氧化生成F,F的相对分子质量为90。
已知:
(1)苯乙醛的分子式为____________;B中具有的官能团有(填名称)_______________。
(2)写出B转化为C反应的化学方程式;该反应类型属反应。
(3)C与H2发生加成反应,1molC最多可消耗H2__________mol。
(4)E可能具有的化学性质有(填序号)___________。
①能与H2发生加成反应
②能在碱性溶液中发生水解反应
③能与甲酸发生酯化反应
④能与Ag(NH3)2OH溶液发生银镜反应
(5)B的同分异构体有多种,其中符合下列要求的有机物有________种;请写出其中一种同分异构体的结构简式。
①与B具有相同的官能团种类
②遇三氯化铁溶液不显色
③苯环上的一氯代物只有两种
(13分)A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,A与C、B与 D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同,A与E形成的化合物化学式为AE,其分子中含18 个电子。请回答下列问题:
(1)A元素单质的化学式为,D元素的离子结构示意图为___。
(2)写出C、D、E最高价氧化物对应水化物的化学式、、(用化学式表示)。
(3)由B元素形成的单质的结构式可表示为___。
(4)由A、B、C三种元素形成的化合物的电子式为___,这种化合物中所含的化学键类型有。
(5)比较D、E的气态氢化物与HF的稳定性的由强到弱的顺序为(用化学式表示)。
(9分)一种常用融雪剂的主要成分的化学式为XY2,X原子的结构示意图为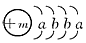 ,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
(1)m=________,该融雪剂的化学式为________。
(2)W元素的名称为________,H2Z的结构式是________。
(3)下列说法正确的是________。
| A.XY2和WZ2都为离子化合物 | B.XY2中仅含离子键,WZ2中仅含共价键 |
| C.H2Z比HY的稳定性强 | D.X的阳离子比Y的阴离子半径大 |
(4)Y元素的单质与H2Z水溶液反应会将Z单质置换出来,请写出该反应的化学方程式,氧化性比较:ZY2(填“>”或“<”)。