.实验探究:为了研究同周期元素性质递变规律,某同学自己设计了一套实验方案,并动手记录实验步骤和现象如下:(表中的“实验步骤”与“实验现象”前后不一定是对应关系)
| 实验步骤 |
实验现象 |
| ① 将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 |
B.有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 |
C.剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 |
D.反应不十分剧烈;产生无色气体。 |
| ⑤向A1Cl3溶液中滴加NaOH溶液至过量 |
E.生成白色胶状沉淀,继而沉淀消失 |
请你帮助该同学整理并完成实验报告:
(1)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、AlC13溶液、NaOH溶液、酚酞溶液等。
实验所用到的玻璃仪器:① 、② 、③ 以及胶头滴管、玻璃片等。
(2)实验内容:(填写与实验步骤对应的实验现象的编号和②的化学方程式)
| 实验内容 |
① |
② |
③ |
④ |
⑤ |
| 实验现象(填A~F) |
B |
|
|
|
|
(3)此实验的结论:钠、镁、铝的金属性强弱 。
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入__________,目的是__________。
(2)反应中加入过量的乙醇,目的是__________________________。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是
______________________________________________________。
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:
则试剂a是:____________,分离方法I是____________,分离方法II是____________,
试剂b是___________ ___,分离方法III是______________。
___,分离方法III是______________。
(5)甲、乙两位同学欲将所得含有乙醇、乙酯和水的乙酸乙酯粗产品提纯, 在未用指示剂的情况下,他们都是先加NaOH溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人实验结果如下:
在未用指示剂的情况下,他们都是先加NaOH溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人实验结果如下:
甲得到了显酸性的酯的混合物
乙得到了大量水溶性的物质
丙同学分析了上述实验目标产物后认为上述实验没有成功。
试解答下列问题:
①甲实验失败的原因是:_______________________________________________
②乙实验失败的原因是:_______________________________________________
制备无水乙醇的实验
原理:由于乙醇95.6%、水4.4%组成一种混合物,常压下,它有一定的沸点(78.17℃),这个沸点低于水的(100℃)也低于纯乙醇的沸点(78.3℃),所以只靠简单蒸馏酒精,所得乙醇纯度最高只能达到95.6%尚含有4.4%的水.如果要得到含量较高的乙醇,在实验室中常用的简便方法是加人生石灰回流(回流是在一个可以加热的反应容器中,把液体加热使受热转化生成的蒸气通过冷凝器冷凝又回流到原容器的操作.见图甲),回流之后再蒸馏,可得99.5%的乙醇,通常称为无水乙醇.如果要得到纯度更高的绝对乙醇(含乙醇99.95%),则还要用金属钠进行处理,借以除去最后微量的水份。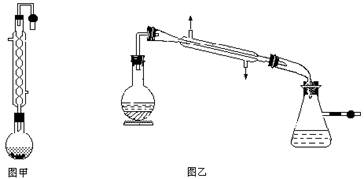
实验步骤::取干燥的250mL圆底烧瓶一只,加入95%乙醇100mL和小块生石灰30g,振摇后用橡皮塞塞紧,放置过夜。在烧瓶口装上回流冷凝管,管口接一支氯化钙干燥管(装置见图甲),在水浴上加热回流1至2小时,稍冷,取下冷凝管,改装成蒸馏装置(如图乙),再放在热水浴中蒸馏,把最初蒸出的5mL馏出液另外回收,然后用烘干的吸滤瓶作为接受器,其侧管接 一支氯化钙干燥管,使其与大气相通,蒸至无液滴出来为止,量取所得乙醇的体积,计算回收率。请回答;
一支氯化钙干燥管,使其与大气相通,蒸至无液滴出来为止,量取所得乙醇的体积,计算回收率。请回答;
(1)为什么回收或蒸馏时都要装上氯化钙干燥管?____________________________
(2)为了防止回流系统外部湿气侵入,有人用塞子把冷凝管上端塞紧,这样做为什么不行?___________________________________________
(3)无水氯化钙常用作吸水剂,如用无水氯 化钙代替氧化钙投入酒精中,放置过夜,然后不经过滤,进行本实验制取乙醇是否可行,为什么?__________________________
化钙代替氧化钙投入酒精中,放置过夜,然后不经过滤,进行本实验制取乙醇是否可行,为什么?__________________________
(4)一般用干燥剂干燥有机物时,在蒸馏前应先过滤,但用氯化钙制备无水乙醇时,为什么可不过滤,留在瓶中一起蒸馏?__________________________________
(5)为什么最初蒸出的5mL馏出液另外收集,它的纯度是否已达99.5%?______________ __________________
氢化钙固体登山运动员常用的能源提供剂。某兴趣小组长拟选用如下装置制备氢化钙。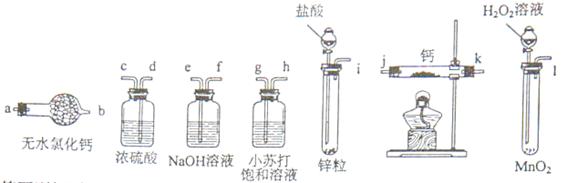
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为________(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞_________(请按正确的顺序填入下列步骤的标号)。
| A.加热反应一段时间 | B.收集气体并检验其纯度 |
| C.关闭分液漏斗活塞 | D.停止加热,充分冷却 |
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此判断,上述实验确有CaH2生成。
__________________
①写出CaH2与水反应的化学方程式 ___________________
②该同学的判断不正确,原因是_________________
(4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象
海洋植物如海带、海藻中含有丰富的碘元素,主要以碘离子形式存在。化学课外小组将海带灼烧成灰,用水浸泡一段时间,得到海带灰悬浊液,然后按以下实验流程提取单质碘I2(已知Cl2可以氧化I-):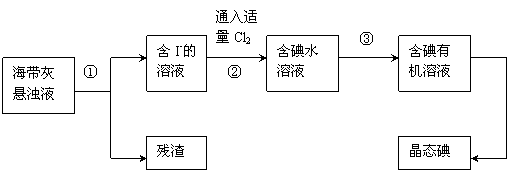
(1)指出提取碘的过程中有关的实验操作名称:③____________,____________;
(2)③提取碘的过程中,可供选择的有机溶剂是____ ___(填字母代号);
___(填字母代号);
| A.酒精 | B.CCl4 | C.汽油 | D.醋酸 |
(3)为使海带灰中碘离子转化为碘的有机溶液,实验室里的烧杯、玻璃棒、
集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器和物品,仍缺少的玻璃仪器________。
(4)步骤②中发生的离子反应方程式为_______________________。
(5)若从含碘的有机溶液中提取碘和回收有机溶剂,还需要经过蒸馏,观察下图实验装置错误之处(有两处),并加以改正_______________________________。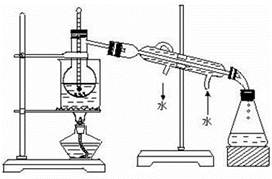
酸碱中和滴定常用于测定酸碱溶液的浓度。
(1)实践中,在正式测定前,常常用已知浓度的酸(或碱)滴定已知浓度的碱(或酸),测定滴定曲线,然后选择合适的指示剂指示滴定终点,以保证数据的准确性。如:用0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L醋酸(CH3COOH) 溶液,有关数据记录如下表:
| V/(NaOH)/mL |
0.00 |
10.00 |
18.00 |
19.80 |
19.98 |
20.00 |
20.02 |
20.20 |
22.00 |
40.00 |
| 溶液pH |
2.87 |
4.74 |
5.70 |
6.74 |
7.74 |
8.72 |
9.70 |
10.70 |
11.70 |
12.50 |
①根据上表数据绘制0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L醋酸(HAc)溶液的滴定曲线。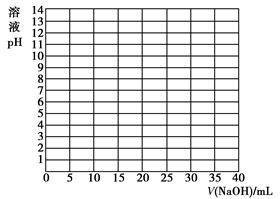
②根据你所绘制的曲线,确定pH的突变范围是________。
③下列指示剂中适合于本实验的是________。(填序号)
A.甲基橙 B.石蕊 C.酚酞
判断到达滴定终点的实验现象
(2)滴定过程中,眼睛应重点观察__。