CrO3主要用于电镀工业,做自行车、仪表等日用五金电镀铬的原料。CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。
请回答下列问题:
(1)B点时剩余固体的化学式是____________。
(2)加热至A点时反应的化学方程式为______________________________。
(3)CrO3具有两性,写出CrO3溶解予KOH溶液的反应化学方程式____________________。
(4)三氧化铬还用于交警的酒精测试仪,以检查司机是否酒后驾车。若反应后红色的CrO3变为绿色的Cr2(SO4)3,酒精被完全氧化为CO2,则其离子方程式为_______________。
(5)由于CrO3和K2Cr2O7均易溶于水,所以电镀废水的排放是造成铬污染的主要原因。某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如图:
①A为电源___________极,阳极区溶液中发生的氧化还原反应为________________________。
②已知电解后阳极区溶液中c(Fe3+)为2.0×10-13 mol·L-1,则c(Cr3+)为__________mol·L-1。{已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31}
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH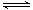 CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)常温常压下,在 pH =5的稀醋酸溶液中,c(CH3COO-)=_________(填数字表达式)。
下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是____(填字母)。
a.加入少量0.10 mol·L-1的稀盐酸 b.加热
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V盐酸______V醋酸 ,(填“>”、“<”或“=”下同),反应的最初速率为:υ盐酸_______υ醋酸。
(3)常温下,向体积为Va mL,pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:_____________;溶液中各离子的浓度按照由大到小排序为_______。
.草酸亚铁晶体(FeC2O4·2H2O)常用作分析试剂及显影剂等。下图是将一定质量的草酸亚铁在氩气氛围中进行热重分析的示意图(TG%表示残留固体质量占原样品质量的百分数)。请回答下列问题:
(1)B处残留物的化学式为。C处残留物的化学式为。
(2)A→C整个反应过程中总反应的化学方程式为。
(3)上述FeC2O4·2H2O在氩气气氛中进行热重分析的原因是。
若将分解得到的600℃时的固体与足量的浓硫酸反应后,将溶液浓缩、冷却,有带9个结晶水的晶体析出,该晶体的化学式为。
(4)现取1.44gFeC2O4放在某真空的密闭容器中,再充入0.04molCO,加热至1100℃,其中反应:FeO(s) + CO(g) 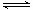 Fe(s) + CO2(g)的平衡常数K=1/3,则反应达平衡时FeO的转化率为。
Fe(s) + CO2(g)的平衡常数K=1/3,则反应达平衡时FeO的转化率为。
写出下列基团(或官能团)的名称或结构简式:
-CH2CH3 、-OH 、异丙基: 、醛基 、羧基 、
为了测定某有机物A的结构,做如下实验: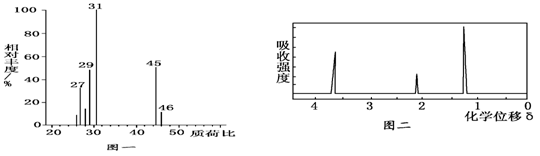
①将9.2g该有机物完全燃烧,生成0.4 mol CO2和10.8 g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1∶2∶3.试回答下列问题:
(1)有机物A的相对分子质量是________.(2)有机物A的实验式是________.
(3)能否根据A的实验式确定A的分子式________(填“能”或“不能”),若能,则A的分子式是________(若不能,则此空不填).(4)写出有机物A可能的结构简式_______.
某有机物由C、H、O三种元素组成,它的红外吸收光谱表明有羟基O-H键和烃基C-H键的红外吸收峰,且烃基与羟基上氢原子个数比为2:1,它的相对分子质量为62,试写出该有机物的结构简式。