(15分)苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理、有关数据及装置示意图如下:
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在三颈瓶中加人2.7 mL甲苯、100 mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加人8.5 g高锰酸钾,继续搅拌约4~5h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。[来
二、分离提纯
在反应混合物中加人一定量草酸(H2C204)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取mg产品,配成100 mL乙醇溶液,移取25.00 mL溶液于锥形瓶,滴加2~3滴酚酞,然后用标准浓度KOH溶液滴定。
请回答下列问题:
(1)装置a的名称是____,其作用为_________
(2)甲苯被高锰酸钾氧化的原理为: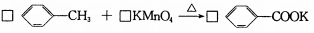

请完成并配平该化学方程式。
(3)分离提纯过程中加人的草酸是一种二元弱酸,反应过程中有酸式盐和无色气体生成。加人草酸的作用是 ,请用离子方程式表示反应原理
(4)产品减压过滤时用冷水洗涤的原因是
(5)选用下列 操作,可以将粗产品进一步提纯。(选填字母)
| A.溶于水后过滤 | B.溶于乙醇后蒸馏 |
| C.用甲苯萃取后分液 | D.升华 |
(6)测定纯度步骤中,滴定终点溶液的颜色变化是____。若m="1.200" g,滴定时用去0.1200 mol· L-1标准KOH溶液20.00 mL,则所得产品中苯甲酸的质量分数为
某同学应用如图所示的方法研究物质的性质,其中气体a的主要成分是氯气,杂质是空气和水蒸气.
回答下列问题:
(1)该项研究(实验)的主要目的是__________________________________________.
(2)浓硫酸的作用是____________________________________________,与研究目的的直接相关的实验现象是________________________________________.
(3)从物质性质的方面来看,这样的实验设计存在着事故隐患,事故表现是___________,请在图中D框中以图的形式表明克服事故隐患的措施.
某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
【提出猜想】
猜想1:_______________________________________________
猜想2:________________________________________________
猜想3:________________________________________________
为了验证猜想,该小组设计实验加以探究:
【实验探究】
该小组同学按如图所示装置,将气体从a端通入,则: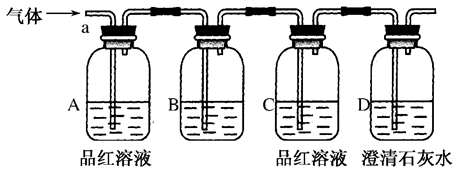
(1)B中应该装下列________试剂(填编号)。
| A.NaCl溶液 | B.酸性KMnO4溶液 |
| C.盐酸 | D.澄清石灰水 |
(2)A中品红溶液的作用是:_________________________________________________。
(3)D中澄清石灰水的作用是:_________________________________________________。
通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色 ②C中品红溶液不褪色
③D中澄清石灰水变浑浊
【得出结论】
(4)由上述现象该小组同学确认该气体的成分为:________。
某课外活动小组的同学在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫;而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两同学的判断是否正确,丙同学设计了如图所示的实验装置(锌与浓硫酸共热时产生的气体为X,且该反应装置已略去):
试回答:
(1)上述实验中生成二氧化硫气体的化学反应方程式为
___________________________。
(2)乙同学认为还可能产生氢气的理由是____________________ _____________________________________。
(3)丙同学在安装好装置后,必不可少的一步操作是____________________________________________。
(4)B中加入的试剂是________,其作用是___________________ _____________________________________。
(5)可以证明气体X中含有氢气的实验现象是:C中________,D中________。如果撤去装置B,是否还能根据D中的现象判断气体X中含有氢气?
答:________,理由是___________________________________
实验室模拟合成氨和氨催化氧化的流程如下:
已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从下图中选择制取气体的合适装置:氮气________、氢气________。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有______________________、____________________________。
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,________(填“会”或“不会”)发生倒吸,原因是_____________。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,锥形瓶中还可观察到的现象是________________。
(5)写出乙装置中氨氧化的化学方程式:__________________。
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、________、________。
甲、乙、丙三位同学分别用如下实验装置及化学药品[碱石灰(氢氧化钠和生石灰的混合物)]制取氨气。请你参与探究,并回答问题:
(1)他们制取氨气的化学方程式为:________________________ _______________________________________________。
(2)三位同学都用向下排空气法收集氨气,其原因是_________ ___________________。
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(实验操作都正确),你认为没有收集到氨气的同学是________填(“甲”、“乙”或“丙”)。
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的的是________(填“甲”、“乙”或“丙”)。