(12分)(1)为测定一种气态烃A的化学式,取标准状况下一定体积的A置于密闭容器中,再通入一定体积的O2,用电火花引燃,定性实验表明产物是CO2、CO和水蒸气。相关方案如下:(箭头表示气体流向,实验前系统内空气已排除)
试回答(不要求写计算过程):
A的实验式(最简式)是___________,根据所学知识,气态烃A的分子式为___________。
(2)质子核磁共振(PMR)是研究有机物结构的有力手段之一,在所研究的化合物分子中,每一个结构中的等效氢原子的PMR谱中都给出了相应的峰(信号),谱中峰的强度与结构中的等效氢原子数成正比。现有某有机物,化学式为C6H12。已知该物质可能存在多种结构,a、b、c是其中的三种,请根据下列要求填空:
①a与氢气加成生成2―甲基戊烷,则a的可能结构有___________种。
②b能使溴水和酸性高锰酸钾褪色,PMR谱中只有一个信号,则b的结构简式为:___ __,
其命名为:
③c不能使酸性高锰酸钾溶液褪色,不能与溴水加成褪色,可萃取溴水中的溴;PMR谱中也只有一个信号,则c的结构简式为:___________________________
燃烧法是测定有机化合物化学式的一种重要方法。在一定温度下取0.1 mol某气态烃A在O2中完全燃烧,生成CO2和水蒸汽,放出热量Q kJ,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重7.2 g,碱石灰增重17.6 g。将烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色。
kJ,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重7.2 g,碱石灰增重17.6 g。将烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色。
(1)写出烃A的分子式 ;
(2) 已知烃A分子结构高度对称且有两个甲基,请写出烃A的结构简式 ;
(3)写出烃A使Br2的CCl4溶液褪色的化学方程式 ;
(4)烃A在一定条件下可以通过加聚反应合成一种塑料,则该反应的化学方程式是 。
某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为。
(2)A可与溴的四氯化碳溶液反应,写出A的结构简式。
(3)已知: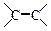

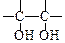 。则A与稀、冷的KMnO4溶液在碱性条件下反应产物的结构简式可表示:。
。则A与稀、冷的KMnO4溶液在碱性条件下反应产物的结构简式可表示:。
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式。
下图为苯和溴取代反应的改进实验装置。其中A为带支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑。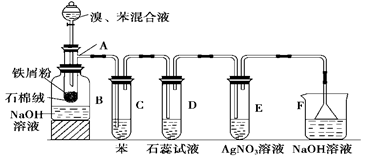
填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式): ,该反应的类型为 反应。
(2)试管C中苯的作用是 ;反应开始后,观察D试管,看到的现象为 ;能说明苯与溴发生的是取代反应而不是加成反应的现象为 。
(3)在上述整套装置中,具有防倒吸作用的仪器有 (填字母)。
(4)实验结束后,得到粗溴苯要用如下操作提纯,①蒸馏;②水洗;③用干燥剂干燥;④用10% NaOH溶液洗;⑤分液。正确的操作顺序是()
| A.⑤④②①③ | B.④②⑤③① | C.④②⑤①③ | D.④⑤③①② |
用一只量筒收集CH4和Cl2的混合气倒扣在盛水的水槽中,用灯光照射量筒中的混合气体,一段时间后,可以观察到量筒内气体颜色,量筒壁上出现
,量筒内水面,量筒中的水溶液呈性。该反应的化学方程式是
(只写第一步)。
 已 知C分子结构中只含有一种氢。F为高分子化合物,结构为:
已 知C分子结构中只含有一种氢。F为高分子化合物,结构为: ,其他物质转化关系如下:
,其他物质转化关系如下:
乙苯+Cl2———→ A ———→ B —
⑤ F
C + Br2——③→ D ———→ E —
(1) C的结构简式是:,名称为:E的键线式为:
(2)框图中属于取代反应的是(填数字代号):
(3)写出②反应进行所需条件:
(4)写出反应④的化学方程式: