在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计,实施和评价,并得出有关结论.
(1)探究稀硫酸与氢氧化钠溶液的反应:
当滴入几滴酚酞试液后,溶液由无色变为 色,根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为: .
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
| 实验方案 |
实验步骤 |
实验现象 |
实验结论 |
| 方案一 |
取样,滴入适量的氯化钡溶液 |
出现白色沉淀 |
稀硫酸过量 |
| 方案二 |
取样,滴入几滴紫色石蕊试液 |
溶液变红 |
稀硫酸过量 |
上述设计的实验方案中,正确的是 (填“方案一”或“方案二”)
另外一个实验方案错误的原因是 ;
请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是 ,实验现象及结论是 .
同学们在实验室用5%的
溶液制取氧气并进行氧气性质实验。
溶液配制:用
30%的
溶液制取氧气(密度为1.13
)配制5%的
溶液(密度约为
)。溶液配制过程中,除用到玻璃棒外还需用到下列仪器中的。
| A. |
托盘天平 |
B. |
烧杯 |
C. |
漏斗 |
D. |
量筒 |
E. |
胶头滴管 |
气体制备:用配制好的5%
溶液和
制取
。请你在"
"、"
"两套装置中选择其中一套,并说明选择的理由,该反应的化学方程式为。待反应结束后同学们回收了混合物中的
,实验操作为。
性质实验:小明用收集好的氧气,进行了下面的实验:
把点燃的木炭伸入集气瓶中,实验现象是;为使铁丝在氧气中持续剧烈燃烧,他把光亮的细铁丝盘成螺旋状,,缓慢插入集气瓶中,观察到持续剧烈燃烧。通过实验得出,氧气可以支持燃烧,并且可燃物燃烧更剧烈。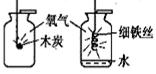
某些食品的包装袋内,放有装有白色固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”。某同学对一袋久置在空气中的干燥剂进行了探究。
他先取部分久置的干燥剂倒入适量水中,充分搅拌、过滤,得到白色固体和滤液。然后对滤液的酸碱性和白色固体的组成作了探究。
【实验探究一】探究滤液的酸碱性
该同学测定了滤液的酸碱性,你认为该滤液显(填“酸性”、“碱性”或“中性”)。
【实验探究二】探究白色固体的组成
该同学认为白色固体中可能含有的物质是CaO、Ca(OH)2、CaCO3。
他查阅有关资料得知:
CaO是一种白色固体,俗称生石灰,能与水反应生成氢氧化钙,并放出热量。氢氧化钙微溶于水。
【分析判断】你认为该白色固体中一定不含有的物质是。
【实验操作】下面是该同学设计的进一步探究白色固体组成的实验方案,请你和他一起完成实验报告。
| 实验操作 |
实验现象 |
实验结论 |
| ①取少量白色固体,倒入适量水,充分搅拌、静置; ②向上层清液中滴加无色酚酞溶液 |
上层清液呈现色 |
白色固体中一定含有 氢氧化钙 |
另取少量白色固体放入试管中,滴加稀盐酸 |
白色固体中一定含有碳酸钙 |
【总结反思】
(1)只通过以上实验,还不能证明这袋久置于空气中的干燥剂是否含有CaO。请用化学方程式表示原因。
(2)请你简述一个证明这袋干燥剂中含有较多量CaO的简易实验:
。
小明为探究
、
、
的金属活动性顺序,做了如下两个实验。请分析实验,完成填空。
(1)试管①中观察到的现象是:铝丝表面附着一层固体,溶液颜色变浅。
(2)试管②中发生了化学反应,现象明显,该反应的化学方程式是。
(3)通过实验探究,
、
、
三种金属活动性由强到弱的顺序是。
李兴同学将
溶液与
溶液混合,得到一种浊液,该反应的化学方程式为。李兴又将浊液过滤,并探究滤液的成分。
【提出猜想】
猜想1:滤液里的溶质只有
;
猜想2:滤液里的溶质有
;
猜想2:滤液里的溶质有
和。
【设计验证实验】
操作I:滤液 验证猜想2
验证猜想2
操作II:滤液 验证猜想3
验证猜想3
其中操作不能达到实验目的,应该将药品更换成(填序号)。
| A. | 溶液 | B. | 溶液 |
| C. | 固体 | D. | 金属铝 |
四硫化钠(
)固体可替代红磷测定空气中氧气的体积分数,反应原理为:
。
【实验资料】
①受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢(水溶液呈酸性)。
②硫代硫酸钠(
)可溶于水,常温下与 溶液不反应。
【实验过程】
①碳酸钠、硫粉混合后置于试管中,加热(如图1所示,夹持装置已略去),制得
,反应
,
的化学式为,蘸有浓
溶液的棉花的作用是。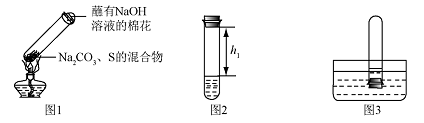
②冷却后,取下棉花,入置一段时间,再向该试管中加入
水,迅速塞紧橡胶塞,充分振荡,测量液面至橡胶塞下沿的距离,记录数据
(如图2所示)
③将该试管插入水中(如图3所求),按下橡胶塞,观察到,塞紧橡胶塞。将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据
,理论上
=
④按照①--③再重复实验
次。
次实验数据如下表所示。
| 第1次 |
第2次 |
第3次 |
|
【解释与结论】根据第1次实验数据,计划空气中氧气的体积分数为
(结果精确到
)
【反应与评价】若实验过程②中,取下棉花后,未放置一段时间即进行后续操作,会影响测定结果,请说明有何影响,并阐述理由:。