(8分)实验探究是体验知识的产生和形成过程的基本途径。下面是某同学完成的探究实验报告的一部分:
实验名称:卤素单质的氧化性强弱比较
| 实验步骤 |
实验结论 |
| ①氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
|
| ③KI溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
实验药品:KBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸
实验设计如下,请回答:
(1)完成该实验需用到的实验仪器是________、________。
(2)②中反应的化学方程式为________________。
③中反应的离子方程式为__________________。
(3)CCl4在实验中所起的作用是________。
(4)该同学的实验设计不足之处是___________________,改进的办法是____________。
实验室制取硝基苯的主要步骤如下:
① 配置一定比例的浓硫酸和浓硝酸的混合物,加入反应器
② 向室温下的混合液中逐滴加入一定量的苯,充分振荡,混合均匀
③ 在50-60℃条件下发生反应,直到反应结束
④ 除去混合酸后,粗产品依次用蒸馏水和5﹪NaOH溶液洗涤,最后用蒸馏水洗涤
⑤ 将用无水CaCl2干燥后的粗硝基苯进行蒸馏得到纯硝基苯
填写下列空白:
① 配置一定比例的浓硫酸和浓硝酸的混合液时,操作注意事项是
② 步骤③中,为了使反应在50-60℃下进行,常用的方法是。
③ 步骤④中洗涤、分离粗硝基苯使用的仪器是。
④ 步骤④中粗产品用5﹪NaOH溶液洗涤的目的是。
⑤ 此反应可表示为。
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下: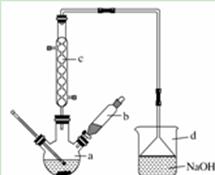
| 苯 |
溴 |
溴苯 |
|
| 密度/g·cm-3 |
0.88 |
3.10 |
1.50 |
| 沸点/℃ |
80 |
59 |
156 |
| 水中溶解度 |
微溶 |
微溶 |
微溶 |
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了_______气体。继续滴加至液溴滴完。装置d的作用是________;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是_____;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是___________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必需的是________(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是________ (填入正确选项前的字母)。
A.25 mL B.50 mL C.250 mL D.500 mL
实验室用浓硫酸和乙醇制取乙烯时,常会看到烧瓶中液体变黑,并在制得的乙烯中混有CO2、SO2等杂质。某课外小组设计了如下装置,证明乙烯中混有CO2、SO2并验证乙烯的性质。
回答下列问题:
(1)装置A是乙烯的发生装置,图中一处明显的错误是______________________,烧瓶中碎瓷片的作用是_____________________________。
(2)若要检验A中所得气体含有SO2,可将混合气体直接通入________(填代号,下同)装置;若要检验A中所得气体含有CH2=CH2,可将混合气体先通过B装置,然后通入________装置,也可将混合气体干燥后,通入________装置。
(3)小明将从A出来的混合气体依次通过B、E、D、E,发现D前面的石灰水无明显变化、D后面的石灰水变混浊。请对出现该现象的原因进行合理猜想:
________________________________________________________________________。
(4)用离子方程式说明SO2使溴水褪色的原理___ _____。
(共8分)过氧化氢水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的浓度, 请填写下列空白:
(1)将10.00 mL过氧化氢溶液移至250mL ___________(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数和化学式分别填在下列横线和括号内。
MnO4- +H2O2+H+="===" Mn2++H2O+( )
(3)移取10mL过氧化氢溶液可以用_______(填“酸式”或“碱式”)滴定管。滴定到达终点的现象是___ 。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的浓度为________。
(5)若盛装高锰酸钾标准溶液的滴定管用蒸馏水洗后没有用标准液润洗,则测定结果______(填“偏高”或“偏低”或“不变”)。
如下图是实验室制备SO2并验证SO2某些性质的装置图。试回答: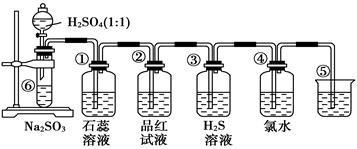
(1)⑥中发生的化学反应方程式为_____________________________。
(2)②中实验现象是,③中反应产物的化学式是
(3)⑤的作用是_____________________,反应的离子方程式为___________________。