(8分)已知X元素的原子K、L层电子数之和比L、M层电子数之和多1个电子。Y元素的原子最外层电子数比内层电子数少3个。Z元素原子核外有3个电子层,最外层有3个电子。回答下列问题:
(1)这三种元素的元素符号是:X________,Y________,Z________。
(2)用电子式表示X、Y形成化合物的过程为________。
(3)把X的单质放入水中,反应现象为___________,高温灼烧反应后的溶液时,火焰呈________色。
(4)当两个Y原子间形成化学键时要________热量。
(5)Y与Z形成化合物的化学式为________;实验测得,当此化合物在液态或固态时不导电,溶解于水时能导电,由此判断该化合物属于________化合物。
用规范的化学语言回答下列问题:
(1)过氧化钠跟CO2反应的化学方程式。
(2)一定条件下,乙醛可跟氢气反应生成乙醇,该反应的反应类型是。
(3)氯化铵溶液呈酸性的原因(用离子方程式回答)。
(4)氢氧化镁浊液中的溶解沉淀平衡方程式。
(5)氯碱工业中用电解饱和食盐水的方法制取烧碱和氯气,该电解过程中的电极反应方程式为:阳极,阴极。
稀盐酸与铝发生反应,要生成3.36L氢气(标准状况),需消耗铝g;反应过程中转移mol电子。
电浮选凝聚法是工业上采用的一种污水处理方法下图是电解污水装置示意图。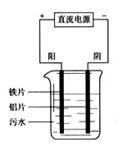
(1)根据污水净化原理写出阳极和阴极的电极反应:
阳极:_____________________,_________________,____________________。
阴极:______________________________。
(2)分析最后底层积聚的一层沉渣是如何沉淀的:__________________________________ __。
(3)一些悬浮物是怎样形成浮渣的:___________________________________________________。
测定铜合金中铜的含量,可以用稀硝酸来溶解样品,也可以用双氧水和稀盐酸溶解样品,其反应的化学方程式为: 。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
①写出铜与稀硝酸反应的离子方程式并标出电子转移的方向和数目____________________。
②在铜与双氧水、盐酸的反应中氧化剂是______________________________,若有2 mol的H2O2参加反应,则电子转移的物质的量是_______________。
③用双氧水和稀盐酸溶解样品与用稀硝酸溶解样品相比较,哪种更好?为什么?____________________。
④若称取样品的质量为a g,用足量的双氧水溶解后,剩余残渣经过洗涤干燥称得质量是b g,
则样品中含铜的质量分数为__________。
实验室通常用二氧化锰和浓盐酸反应制取氯气写出反应方程式______________,浓盐酸还可以和氯酸钾发生反应制取氯气写出反应方程式______________,氯气具有较强的__________性。