(18分)甲、乙、丙是常见的三种物质,它们之间有如图所示的转化关系。根据要求回答下列问题:
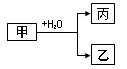
I.已知:甲是由两种短周期元素组成的化合物,丙的水溶液显碱性。
(1)若构成甲的阴、阳离子个数比为2:3,丙是气体。则构成甲的阴、阳离子半径大小关系为 (用具体的微粒表示)。
(2)若乙是O2,则甲的一种重要用途是 ;产物丙与Cl2按2:1(物质的量)反应得到丁溶液,丁溶液中阴离子浓度从大到小的顺序是 。
Ⅱ.一种灰白色固体粉末X是由两种常见元素组成的化合物,其中金属元素与另一元素的质量比为14:l。在一定条件下X可发生如下图转化关系,有的反应标出全部产物,有的反应标出部分产物。已知P为混合气体,R是无色无味能使澄清石灰水变浑浊的气体,C为红褐色物质,M为常见金属单质,Q为常见非金属单质。请回答下列问题:
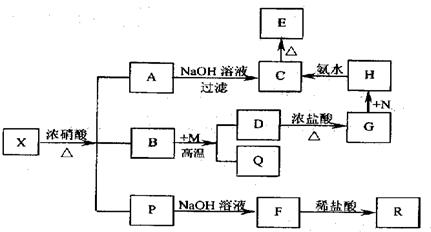
(1)X的化学式为______________;R的电子式为_________________。
(2)写出气体P的组成 。
(3)写出D→G的离子反应方程式 。
(4)M与钛构成的合金是一种常用的不锈钢材料,某同学在探究该合金的性质时,往含有TiO2+、M3+溶液中加入M至溶液显紫色,该过程中发生的反应有:
①2TiO2+(无色)+Fe+4H+==2Ti3+ (紫色)+Fe2++2H2O
②Ti3+(紫色)+Fe3++H2O ="=" TiO2+ (无色)+Fe2++2H+
③ 。
请写出③可能的反应方程式 。
(5)人们对X的结构研究后发现其金属元素有0价、+2价两种化合价,写出X与稀硫酸反应的化学方程式 。
(6)合硫酸M是一种常见的净水剂,化学式为:[M2(OH)n (SO4)3-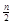 ]m (n>2,m≤10),其制备可由硫酸M经水解后再聚合得到,其中聚合反应的原理为m[M2(OH)n(SO4)3-
]m (n>2,m≤10),其制备可由硫酸M经水解后再聚合得到,其中聚合反应的原理为m[M2(OH)n(SO4)3-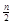 ]
]  [M2(OH)n(SO4)3-
[M2(OH)n(SO4)3-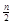 ]m,则写出硫酸M水解的化学方程式为 。
]m,则写出硫酸M水解的化学方程式为 。
简答题( 9分)(1)已知:C2H6O(g) + 3O2(g) ="=" 2CO2(g) + 3H2O(g)△H1
H2O(g)==H2O(l)△H2 ;
C2H6O(g)==C2H6O(l)△H3
若使1mol C2H6O(l)完全燃烧生成液态水,则放出的热量为(用符号表示)
(2)对于可逆反应CO(g)+H2O (g)  CO2(g)+H2 (g),若开始时容器中各有1mol的CO(g)和H2O (g),并在一定条件下发生反应,回答下面的问题:
CO2(g)+H2 (g),若开始时容器中各有1mol的CO(g)和H2O (g),并在一定条件下发生反应,回答下面的问题:
①恒温恒压时,向容器中充入0.5mol的He,这时反应速率(填“加快”、“减慢”或 “不变”),原因是
②恒温恒容时,加入0.3mol的CO,这时反应速率(填“加快”、“减慢”或 “不变”),原因是。
简答题(7分)t℃时,将2molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g),ΔH= -196.6kJ/mol。2min时反应达到化学平衡,此时测得反应物O2还剩余0.8mol,请填写下列空白:
2SO3(g),ΔH= -196.6kJ/mol。2min时反应达到化学平衡,此时测得反应物O2还剩余0.8mol,请填写下列空白:
(1)从反应开始到达化学平衡,生成SO3的平均反应速率为;平衡时SO2浓度为;
(2)下列叙述能证明该反应已达到化学平衡状态的是(填标号);
| A.容器内气体的总压强不再发生变化 |
| B.SO2的体积分数不再发生变化 |
| C.容器内气体原子总数不再发生变化 |
| D.相同时间内消耗2nmolSO2的同时消耗nmolO2 |
E.相同时间内消耗2nmolSO2的同时生成nmolO2
填空题( 6分)(1) ①C(s) + O2(g) ="=" CO2(g);ΔH= –393.5kJ/mol
②CO(g) + 1/2 O2(g) ="=" CO2(g);ΔH= –283kJ/mol
根据上述信息,写出C转化为CO的热化学方程式为____________________________。
(2)已知CH4的燃烧热为890kJ/mol,则24g CH4完全燃烧放出的热量为。
填空题( 24分)(1)25℃、101 kPa下,1 mol 氢气燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为___________________________________________________。
(2) 25℃,101kPa时,16 g CH4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出890.3 kJ热量,则CH4燃烧的热化学方程式为_______________________________________________。
(3)25℃,101kPa时,0.5 mol CO在足量的O2中充分燃烧,放出141.3 kJ的热,则CO的燃烧热为,其表示燃烧热的热化学方程式是。
(4)0.50L 2.00mol/L H2SO4与2.00L 1.00mol/L KOH溶液完全反应,放出114.6kJ的热量,该反应的中和热为,其表示中和热的热化学方程式为。
(5)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391 kJ、946 kJ,则25℃,101kPa时,N2与H2反应生成NH3的热化学方程式是。
用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A,可实现氯的循环利用。反应A: 4HCl+O2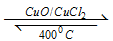 2Cl2+2H2O。
2Cl2+2H2O。
(1)已知:i 反应A中, 4mol HCI被氧化,放出115.6kJ的热量。
ii
①H2O的电子式是_______________.
②反应A的热化学方程式是____________________________________________________。
③断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________kJ,H2O中H—O 键比HCl中H—Cl键(填“强”或“弱”)_______________。
(2)对于反应A,下图是4种投料比[n(HCl):n(O2),
分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。
①曲线b对应的投料比是__________。
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度高低与投料比多少的关系是______________________________。
③投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数__________。