本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.【改编】锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu的核外电子排布式: 。
(2)SO42—的空间构型是 。
(3)NH3分子中氮原子轨道的杂化类型是 。
(4)氮元素的一种氢化物肼(N2H4)是火箭燃料,则1 molN2H4中含有的σ键的数目为 。
(5)铜的配合物[Cu(CN)4]2-中含有CN-,写出与CN-互为等电子体的一种分子为 (填化学式)。
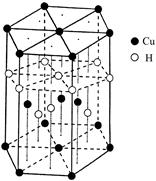
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式为 。
“西气东输”是西部开发的重点工程,这里的“气”是指天然气,其主要成分是甲烷。水煤气中主要成分是CO和H2,二者的体积比为l :l。已知:在120℃和一个大气压下,H-H键能为436 kJ/mol,O=O键能为496 kJ/mol,H-O键能为463 kJ/mol ;1 mol CO气体完全燃烧生成CO2气体放出283 kJ热量;l mol CH4气体完全燃烧生成CO2气体和气态水放出802 kJ热量。
(1)写出120℃和一个大气压下,H2完全燃烧生成气态水的热化学方程式;
(2)相同条件下,若l mol CH4气体完全燃烧生成CO2气体和液态水,放出的热量802 kJ;(选填“>”、“=”、“<”)
(3)忽略水煤气中其他成分,燃烧等体积的CH4和水煤气,所得热量之比约为;
(4)请结合以上计算结果,叙述相比于水煤气,天然气作为燃料的两个优点:
。
某学生为了探究Zn与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的Zn粉,用排水集气法收集反应放出的H2,实验记录如下(累计值):
| 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大,你认为原因是;
(2)4~5 min时间段的反应速率最小,你认为原因是; (3)求2~3 min时间段内以盐酸的浓度变化来表示的反应速率(假设溶液体积保持不变)V(HCl)=;
(3)求2~3 min时间段内以盐酸的浓度变化来表示的反应速率(假设溶液体积保持不变)V(HCl)=;
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
| A.H2O | B.NaCl溶液 | C.Na2CO3溶液 | D.Cu粉E.CuSO4粉末; |
你认为可行的是(填编号)。
有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同。
请回答下列问题: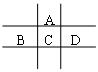
(1)B元素在周期表中的位置为;
(2)A与氢元素能形成原子物质的量之比为1:1的化合物,其电子式为;
(3)向D与E形成的化合物的水溶液中滴入NaOH溶液直至过量,观察到的现象是,最后阶段反应的离子方程式为 ;
(4)B、C、D、E的最高价氧化物的水化物的酸性从强到弱的顺序为(物质用化学式表示)。
有下列一组物质:He、Cl2、CH4、Na2O2、Ba(OH)2、NO2、KNO3、H2SO4,请从中选择,用化学式填写下列空白:
(1)只含有共价键,不含其他化学键的化合物有;
(2)既含有共价键又含有离子键的物质有;
(3)能在水中发生氧化还原反应的有。
某微粒的结构示意图为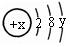 试回答:
试回答:
(1)当x-y=10时,该粒子为(选填“原子”或“阳离子”、“阴离子”);
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)、、;
(3)请写出工业上制取y=7元素对应单质时的离子方程式:
。