【改编】【物质结构与性质】Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
| 元素 |
Mn |
Fe |
|
| 电离能kJ/mol |
I1 |
717 |
759 |
| I2 |
1509 |
1561 |
|
| I3 |
3248 |
2957 |
|
回答下列问题:
(1)Mn元素核外电子的电子排布式为 ,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。其原因是 。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①Fe原子或离子易形成配合物的原因是 ,与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 。
②络离子[Fe(CN)6]4-的配体CN-中C原子的杂化轨道类型是 ,HCN的分子构型为 ,写出一种与 CN-互为等电子体的单质分子的电子式 。
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体构成微粒为 。
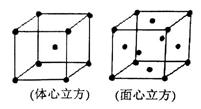
(4)金属铁晶体在不同的温度下有两种堆积方式,如图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为 。
(1)1.204×1024个氯化氢分子的物质的量为________;将其溶于水配成5L溶液,该溶液物质的量浓度为________;
(2)含0.4 mol Al3+的Al2(SO4)3的物质的量是___________,所含的SO42-的物质的量是___________。
硫及其部分化合物的转化关系如图所示。
(1)通常状况下硫单质的颜色为_________。
(2)SO2可以使品红溶液褪色,说明SO2具有_________(填“漂白性”或“氧化性”)。
(3)化合物A的化学式为__________。
(4)反应⑤的离子方程式为___________________________。
(5)反应④中,当32g Cu完全反应时,被还原的H2SO4的物质的量为________mol。
某些铁、铝制品的表面常生成一层氧化物,其主要成分分别是氧化铁、氧化铝。两种氧化物均能与盐酸反应,生成的两种盐的化学式分别为_____________、____________。向这两种盐的溶液中分别滴加足量氢氧化钠溶液,可观察到:其中一种溶液中的现象是先产生白色沉淀,然后白色沉淀逐渐消失则该溶液为_____________溶液;另一种溶液中的现象是______(填序号)。
①产生白色沉淀
②产生红褐色沉淀
③产生白色沉淀,迅速变成灰绿色,最后变成红褐色
印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,其反应的化学方程式如下:Cu+ 2FeCl3═ CuCl2 + 2FeCl2
(1)指出上述反应中氧化剂是__________,还原剂是__________。
(2)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是_______(填序号)。
| A.氯气 | B.铁 | C.盐酸 | D.稀硫酸 |
在Cl2、NO、SO2、NO2、NH3五种气体中,与空气相遇能立即变色的是_________;
常用于自来水杀菌、消毒的是________;能用向下排空气法收集的是__________;溶于水后能生成强酸的是_________。