(15分)碳酸二甲酯(DMC)是一种近年来受到广泛关注的环保型绿色化工产品。在催化剂作用下,可由甲醇和CO2直接合成DMC:CO2 + 2CH3OH → CO(OCH3)2 + H2O,但甲醇转化率通常不会超过1%是制约该反应走向工业化的主要原因。某研究小组在其他条件不变的情况下,通过研究温度、反应时间、催化剂用量分别对转化数(TON)的影响来评价催化剂的催化效果。计算公式为: 。
。
(1)已知25℃时,甲醇和DMC的标准燃烧热分别为△H1和△H2,则上述反应在25℃时的焓变△H3= 。
(2)根据反应温度对TON的影响图(下左图)判断该反应的焓变△H______0(填“>”、“=”或“<”),理由是________________________________。

(3)根据反应时间对TON的影响图(上中图),已知溶液总体积10mL,反应起始时甲醇0.25mol,催化剂0.6×10—5 mol,计算该温度下,4~7 h内DMC的平均反应速率:________;计算10 h时,甲醇的转化率:________。
(4)根据该研究小组的实验及催化剂用量对TON的影响图(上右图),判断下列说法正确的是 。
a.由甲醇和CO2直接合成DMC,可以利用价廉易得的甲醇把影响环境的温室气体CO2转化为资源,在资源循环利用和环境保护方面都具有重要意义
b.在反应体系中添加合适的脱水剂,将提高该反应的TON
c.当催化剂用量低于1.2×10—5 mol时,随着催化剂用量的增加,甲醇的平衡转化率显著提高
d.当催化剂用量高于1.2×10—5 mol时,随着催化剂用量的增加,DMC的产率反而急剧下降
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如右图所示。
(1)如果A是淡黄色固体,
①写出B、E的化学式:B 、E 。
②C→D的化学方程式为_____________________。
③将足量的物质C通过入BaCl2溶液中,下列说法正确的是___________(填字母序号)。
a.溶液没有明显变化
b.溶液中出现白色浑浊
c.若继续通入Cl2或NH3,溶液都出现白色浑浊
(2)如果A是无色气体:
D→E的化学方程式为 ;
E→C的离子方程式为 。
现有6种短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| W |
周期表中原子半径最小的元素 |
| U |
地壳中含量最多的金属元素 |
| R |
单质为空气的主要成分 |
| T |
M层上有6个电子 |
| X |
最外层电子数是次外层电子数的2倍 |
| Y |
氢化物水溶液呈碱性 |
| Z |
元素最高正价是+7价 |
完成下列空白(涉及W、U、R、T、X、Y、Z时,用元素符号表示):
(1)元素T的原子共有个电子;元素X的一种核素可测定文物年代,这种核素的
符号是。
(2)用电子式表示:
①气态化合物XR2_________________;
②元素W、R形成的10电子分子的形成过程______________________________。
(3)用离子方程式表示:
①元素Y与元素W形成的离子YW4+与NaOH溶液共热的反应 _____;
②元素U的单质与NaOH溶液反应_______________________________________。
(4)元素Z与元素T相比,非金属性较强的是,下列表述中能证明这一事实的
是(填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)探寻物质的性质差异性是学习的重要方法之一。在T、X、Y、Z四种元素的最高价
氧化物的水化物中,化学性质明显不同于其他三种的是(用分子式表示),
理由是。
将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题: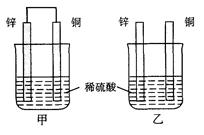
(1)下列说法正确的是____________。
| A.甲、乙均为化学能转变为电能的装置 |
| B.乙中铜片上没有明显变化 |
| C.甲中铜片质量减少、乙中锌片质量减少 |
| D.两烧杯中溶液的pH均增大 |
(2)在相同时间内,两烧杯中产生气泡的速度:甲____乙(填“>”、“<“或“=”)。
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为_______________。
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至
1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫
酸的物质的量浓度为_________________。
填写下列空白:
(1)表示含有17个质子、20个中子的原子的化学符号是___________________。
(2)第三周期0族元素的原子结构示意图为_______________。
(3)周期表中被称为第Ⅷ族的元素位于第_____________________纵行。
(4)周期表中最活泼的非金属元素位于第__________周期、第_________族。
(5)所含元素超过18种的周期是第__________、_________周期。
向一定量的NaOH固体中加入由硫酸铜和硫酸组成的混合物的溶液,充分搅拌,恰好完全反应,有蓝色沉淀生成,过滤,所得滤液的质量与加入的原混合物溶液的质量相等。则与硫酸铜反应的氢氧化钠和与硫酸反应的的氢氧化钠的物质的量之比为。