(16分)碳、氮、硫、氯是四种重要的非金属元素。
(1)CH4(g)在O2(g)中燃烧生成CO(g)和H2O(g)的△H难以直接测量,原因是 。
已知:a.2CO(g)+ O2(g)==2CO2(g) △H =-566.0 kJ·mol-1
b.CH4(g)+2O2(g)==CO2(g)+2H2O(g) △H =-890.0 kJ·mol-1
则CH4(g)在O2(g)中燃烧生成CO(g)和H2O(g)的热化学方程式为 。
(2)工业上合成氨气的反应为:N2(g)+3H2(g) 2NH3(g) △H<0。现将10 mol N2和26 mol H2置于容积可变的密闭容器中,N2的平衡转化率(
2NH3(g) △H<0。现将10 mol N2和26 mol H2置于容积可变的密闭容器中,N2的平衡转化率(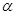 )与体系总压强(P)、温度(T)的关系如图所示。回答下列问题:
)与体系总压强(P)、温度(T)的关系如图所示。回答下列问题: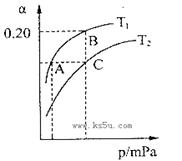
①反应达到平衡状态B时,容器的容积10 L,则T1时,合成氨反应的平衡常数K= L2·mol-1。
②平衡状态由A变到C时,对应的平衡常数K(A) K(C)(填“>”、“<”或“=”)。
(3)在25℃时,HSCN、HClO、H2CO3的电离常数如下表:
| HClO |
HSCN |
H2CO3 |
| K=3.2×10-8 |
K=0.13 |
Kl=4.2×10-7[来源 K2=5.6×10-11 |
①1 mol·L-1的KSCN溶液中,所有离子的浓度由大到小的顺序为 > > > 。
②向Na2CO3溶液中加入过量HClO溶液,反应的化学方程式为 。
③25℃时,为证明HClO为弱酸,某学习小组的同学没计了以下三种实验方案。下列三种方案中,你认为能够达到实验目的的是 (填下列各项中序号)。
a.用pH计测量0.1 mol·L-1NaClO溶液的pH,若测得pH>7,可证明HClO为弱酸
b.用pH试纸测量0.01 mol·L-1HClO溶液的pH,若测得pH>2,可证明HClO为弱酸
c.用仪器测量浓度均为0.1 mol·L-1的HClO溶液和盐酸的导电性,若测得HClO溶液的导电性弱于盐酸,可证睨HClO为弱酸
氯气是一种有毒气体,但它是一种重要的化工原料,与我们的生活联系也比较密切。
(1)据新闻报道,前不久某地装运液氯的槽罐车发生交通事故,造成大量氯气泄漏,公路附近的村民被紧急疏散。请问:村民应该如何应变(填编号)。
| A.应躲到低洼的地方去 | B.可用烧碱溶液浸湿软布蒙面 |
| C.可用肥皂水或尿液浸湿软布蒙面 | D.应多饮水 |
E.应到较高的地方去
(2)实验室制取氯气的方法有很多种,其中之一是:KClO3+6HCl=KCl+3Cl2↑+3H2O。该反应中氧化剂是,还原剂是,当反应生成标准状况下6.72LCl2时,转移电子的物质的量为。
(3)日常生活环境可用稀的漂白液等进行消毒,请写出制漂白液的离子方程式
。
下图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去)。其中A是单质,D在常温下呈气态,F可用作氮肥。
据此,请回答下列问题:
(1)写出物质的化学式:A ,D ,F 。
(2)写出下列变化的化学方程式:
B→C 。
E→C 。
 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反应如下图所示:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧。A的相关反应如下图所示:



 已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO。
已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO。
 根据以上信息回答下列问题:
根据以上信息回答下列问题:
 (1)A的分子式为;
(1)A的分子式为;
 (2)反应②的化学方程式是;
(2)反应②的化学方程式是;
 (3)A的结构简式是
(3)A的结构简式是
 ;(4)反应①的化学方程式是;
;(4)反应①的化学方程式是;
 (5)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为。
(5)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为。
.已知有机物分子中的烯键可发生臭氧分解反应,
例如:R-CH=CH-CH2OH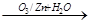 R-CH=O+O=CH-CH2OH。A的部分性质如图所示:
R-CH=O+O=CH-CH2OH。A的部分性质如图所示:
试根据上述信息结合所学知识写出A的结构简式。
氮化硼(
)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到
和
,如下图所示:
请回答下列问题:
(1)由
制备
、
的化学方程式依次是、;
(2)基态B原子的电子排布式为;B和N相比,电负性较大的是,
中B元素的化合价为;
(3)在
分子中,
的建角是,B原子的杂化轨道类型为,
和过量
作用可生成
,
的立体结构为;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为,层间作用力为;
(5)六方氢化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶苞边长为361.5
,立方氮化硼晶苞中含有各氮原子、各硼原子,立方氮化硼的密度是
(只要求列算式,不必计算出数值,阿伏伽德罗常数为
)。