25℃时,下列溶液中微粒的物质的量浓度关系正确的是
| A.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3) |
| B.浓度均为0.1mol/L的HCN和NaCN混合液(pH>7):c(HCN)>c(CN-)>c(Na+)>c(OH-)>c(H+) |
| C.浓度均为0.1mol/L的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) |
| D.CH3COONa溶液和盐酸混合呈中性的溶液中:c(Na+)>c(Cl-)=c(CH3COOH) |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.能使甲基橙变黄的溶液中:Na+、K+、SO42-、Al3+ |
| B.pH=2的溶液中:Na+、ClO-、NH4+、SO42- |
| C.某透明澄清的溶液中:NH4+、Cu2+、NO3-、Cl- |
| D.0.1 mol·L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl- |
下列物质中属于纯净物的是:①由同种元素组成的物质;②具有固定熔沸点的物质;③由相同种类和相同数目的原子组成的分子;④只有一种元素的阳离子和另一种元素的阴离子组成的物质;⑤在氧气中燃烧只生成二氧化碳的物质;⑥只含有一种分子的物质
| A.②③⑥ | B.④⑤⑥ | C.①④ | D.②⑥ |
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是 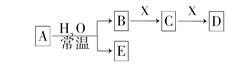
A.若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,则E是一种清洁的能源
B.若D为CO,C能和E反应,则A一定为Na2O2,其电子式是
C.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
D.若X是Na2CO3,C为含极性键的分子,则A一定是氯气,且D和E能发生反应
某含铬[Cr2O72-] 废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀,该沉淀干燥后得到n molFeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是
| A.消耗硫酸亚铁铵的物的质量为n(2-x)mol |
B.处理废水中Cr2O72- 的物质量为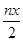 mol mol |
| C.反应中发生转移的电子数为3nx mol |
| D.在FeO·FeyCrxO3中3x=y |
一定量的铝铁合金与300 mL 2 mol/L的硝酸反应生成3.36 L NO(标准状况)和3价铁盐、铝盐等,再向反应后的溶液中加入3 mol/L NaOH溶液,使铝铁元素刚好全部转化为沉淀,则所加NaOH的体积为
| A.100 mL | B.150 mL | C.450 mL | D.无法计算 |