废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧黄铜(Cu、Zn合金,含少量杂质Fe)制备胆矾晶体(CuSO4·5H2O)及副产物ZnO。制备流程图如下:

已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol/L计算)。
| |
Fe3+ |
Fe2+ |
Zn2+ |
| 开始沉淀的pH |
1.1 |
5.8 |
5.9 |
| 沉淀完全的pH |
3.0 |
8.8 |
8.9 |
请回答下列问题:
(1)由不溶物E生成溶液D的离子方程式为______________________________。
(2)加入ZnO调节pH=a的目的是___________________,a的范围是 。
(3)检验滤液D中不存在铁离子的实验操作是 。
(4)由溶液D制胆矾晶体包含的主要操作步骤是 。
(5)下列试剂可作为Y试剂的是______。
A.ZnO B.NaOH C.Na2CO3 D.ZnSO4
(6)测定胆矾晶体的纯度(不含能与I-发生反应的氧化性杂质):准确称取0.5000g胆矾晶体置于锥形瓶中,加适量水溶解,再加入过量KI,用0.1000mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液19.40mL。已知:上述滴定过程中的离子方程式如下:2Cu2++4I-=2CuI(白色)↓+I2,I2+2S2O32-=2I-+S4O62-。
①胆矾晶体的纯度为_________。
②在滴定过程中剧烈摇动(溶液不外溅)锥形瓶,则所测得的纯度将会________(填“偏高”、“偏低”或“不变”)。
用含少量铁的氧化物的氧化铜制取硫酸铜晶体( CuSO4.xH2O)。其流程如下: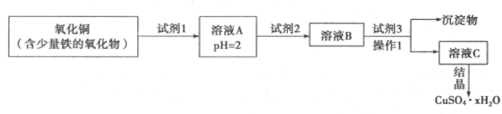
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)溶液A中可能含有Fe2+,确定该溶液中Fe2+存在的试剂是_______(填序号)
| A.H2O2 | B.NaOH | C.K3[Fe(CN)6] | D.KSCN |
(2)欲用(1)中选择的检验试剂测定溶液A中Fe2+的浓度,实验前,首先要配制一定物质的量浓度的检验试剂的溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、药匙、250mL容量瓶外,还需_______,下列滴定方式中,最合理的是_______(夹持部分略去)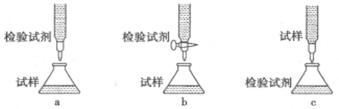
判断达到滴定终点的方法是__________________________________.
写出滴定反应的离子方程式__________________________________.
(3)试剂1为________,试剂2的作用为________,操作1的名称为________。
(4)要得到较纯的产品,试剂3可选用________。
a.NaOH
b.CuO
c.FeO
d.Cu(OH)2
e.Cu2(OH)2CO3
FeSO4·7H2O广泛用于医药和工业领域,实验室制备FeSO4·7H2O的流程如下:
(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_________。
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;②_____________________。
(3)FeSO4·7H2O是某些补血剂的主要成分,实验室用KMnO4溶液通过氧化还原滴定测定某补血剂(1.500 g)中铁元素的含量。
①配制100 mL 1.200 × 10 —2 mol·L—1的KMnO4溶液时,将溶解后的溶液转移至容量瓶中的操作方法是__________________________;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是_________________。
a.稀硝酸b.稀盐酸c.稀硫酸d.浓硝酸
KMnO4溶液应盛装在__________滴定管中。滴定到终点时的现象为_____________________。滴定完毕,三次实验记录KMnO4标准溶液的读数如下。
| 滴定次数实验数据 |
1 |
2 |
3 |
| V(样品)/mL |
20.00 |
20.00 |
20.00 |
| V(KMnO4)/mL(初读数) |
0.00 |
0.20 |
0.00 |
| V(KMnO4)/mL(终读数) |
15.85 |
15.22 |
14.98 |
该补血剂中铁元素的质量分数为_____________________。
(4)某实验小组用久置的FeSO4溶液和NaOH溶液制备Fe(OH)2,实验后没有得到预期的白色沉淀,于是采用下列试剂(已煮沸除氧)和装置进行实验: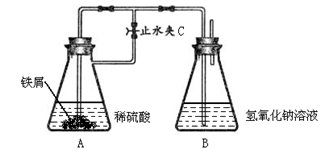
实验开始打开止水夹C,目的是_______________________。一段时间后,关闭止水夹C, B中观察到的现象是______________________。B中发生反应的离子方程式是___________________。
以铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)为原料,可制得液体聚合氯化铝 [Alm(OH)nCl3m—n],生产的部分过程如下图所示(部分产物和操作已略去)。
(1)Al2O3与盐酸反应的离子方程式是_____________________。
(2)滤渣I是__________。滤渣2为黑色,该黑色物质的化学式是___________。
(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。其中NaClO的作用是___________。该过程发生反应的离子方程式为______________。
(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。该反应的化学方程式为_____________________。
(5)Na2S溶液呈碱性的原因是________(用离子方程式表示)。该溶液中c(Na+)=________。
某兴趣小组利用下列实验装置进行探究实验。根据要求回答下列问题:
(1)装置中长颈漏斗的作用有导气、。
(2)利用装置C可以证明S02具有漂白性,C中盛放的溶液是;若要证明其漂白作用是可逆的,还需要的操作是。
(3)通过观察D中现象,即可证明S02具有氧化,D中盛放的溶液可以是。
a.NaCl溶液b.酸性KMn04c.FeCl3d.Na2S溶液
(4)研究小组发现B中有白色沉淀生成,若往B中加入过量稀盐酸,沉淀不溶解。沉淀物的化学式是。
(5)为进一步验证B中产生沉淀的原因,研究小组进行如下两次实验:
实验i:另取BaCl2溶液,加热煮沸,冷却后加入少量苯(起液封作用),然后再按照上述装置进行实验,结果发现B中沉淀量减少,但仍有轻微浑浊。
实验ii:用下图装置代替上述实验中的A装置(其他装置不变),连接后往装置F中通入气体X一段时间,再加入70%H2S04溶液,结果B中没有出现浑浊。
①“实验i”中煮沸BaCl2溶液的目的是;
②气体X不可以是(填序号)。
a.CO2b.O3c.N2d.NO2
③B中形成沉淀的原因是(用化学方程式表示):。
某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案:
(1)小明同学用图中的发生、收集装置。甲、乙两试管各有两根导管,连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体。则稀硫酸应置于中(填“甲”或“乙”);G管可以用化学实验室里的一种常用仪器代替,你认为这种仪器的名称是。仪器甲、乙接口的连接方式如下:A连接,C连接F;(填写接口的编号)
(2)小李同学用沉淀法测定Na2SO3的质量分数。
操作流程:
①操作Ⅱ的名称是。
②操作Ⅰ之前,为判断所加BaCl2溶液是否过量, 设计如下方案,其中最合理的是。
A.取少量上层清液,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
B.待浊液澄清后,继续滴加BaCl2,若无沉淀产生则说明BaCl2已过量。
C.待浊液澄清后,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
③根据以上数据得出Na2SO3的质量分数为。
④小丽同学经认真分析,上述实验操作均正确,但发现实验结果与预期相差较大,请你推测可能的原因是,验证方法。