(9分)金属在生产、生活中有着广泛的用途。
(1)指出金属铁的一个性质及其对应的用途:性质_________,对应用途_________。
(2)黄铜是铜锌合金,其硬度比纯铜_________ (填“大”、“小”或“相同”)。
(3)多数金属在自然界以矿物的形式存在,请写出一种含铁元素的矿石名称 ,用化学方程式表示工业炼铁的原理 。
(4)长期露置于空气中的金属M表面会被锈蚀。经检测,锈蚀物中除含有M外,还含有碳、氢、氧三种元素。根据质量守恒定律,推测与金属M发生反应生成锈蚀物的物质。
推测Ⅰ:锈蚀物中的氢来自空气中的____________(填化学式,下同),碳来自空气中的______________,因此这两种物质肯定参加了反应。
推测Ⅱ:锈蚀物中的氧有多种来源,因此不能确定空气中的氧气是否参加了反应。
(4)某同学为了验证空气中的O2是否参加了反应,设计了如图所示的系列实验,你认为其中必须要做的实验是_________ (填实验编号)。
(说明:①所用蒸馏水都是经煮沸迅速冷却的;②固体干燥剂N只吸收水分,不吸收CO2和O2。)
下图是提纯CO、CO2混合气体中的CO并还原氧化铁的示意图。请回答有关问题: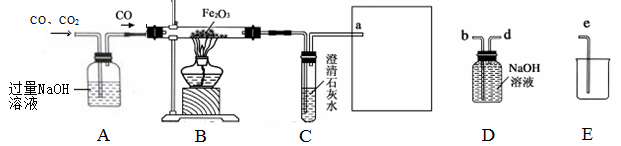
(1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是D和E,导管接口的连接顺序为a→ ()→()→ ()。D装置中NaOH的作用是。
如果导管连接错误,后果是____________ ____________________________。
(2)实验进行一段时间后,B装置的玻璃管中的现象为,反应方程式为。用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是_____________ ____________。
(3)实验结束后,要从A装置的混合溶液中回收得到较纯净的NaOH固体。
资料显示,在不同温度下NaOH的溶解度如下:
| 温度(℃) |
10 |
20 |
40 |
60 |
80 |
100 |
| 溶解度(g/100g水) |
64 |
85 |
138 |
203 |
285 |
376 |
利用实验室的试剂和条件,实验步骤如下(其中Ⅰ、Ⅱ、Ⅲ为实验操作):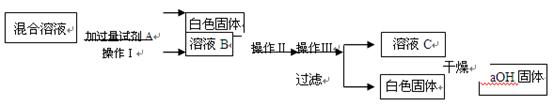

请具体填写试剂A的化学式以及实验操作Ⅰ、Ⅱ、Ⅲ的名称。
①化学式:A_________ ____________;
②操作名称:Ⅰ_________ ________ Ⅱ________ ___________ Ⅲ________ __________。
③如果在操作Ⅱ的过程中,溶液B中出现少量浑浊,原因可能是。
能源“非石油化”是战略目标,发展以CH4、CO2等原料的 “C1化学”成为当今化工生产的必然趋势。通常天然气中含有H2S等有毒气体,下图为天然气合成氨(NH3)的工艺流程: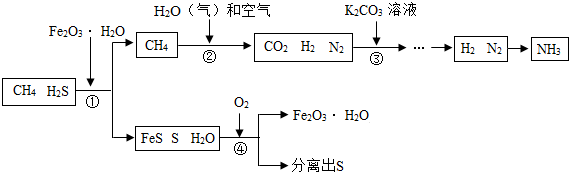
(1)合成氨的原料之一为氮气,该流程中为合成氨提供氮气的物质是。
(2)①处加入Fe2O3·H2O的目的是。
(3)②处CH4与H2O(气)反应生成CO2、H2,反应的化学方程式是(反应条件略去)。
(4)③处一般加入K2CO3溶液以吸收CO2 ,K2CO3溶液与CO2反应生成碳酸氢钾(KHCO3),该反应的化学方程式是 。
(5)该流程中参与循环的物质是。
同学们在实验室进行“粗盐中难溶性杂质的去除”实验。以下是小丽同学的实验报告部分内容。
【实验目的】粗盐中难溶性杂质的去除
【实验过程】
①用托盘天平称取5.0g粗盐,并全部加入到盛有10mL水的烧杯里,边加边用玻璃棒搅拌;
②过滤食盐水,观察滤液无色透明;
③将所得澄清滤液倒入蒸发皿,加热,并用玻璃棒不断搅拌,当液体蒸干时,停止加热;
④用玻璃棒把固体转移到纸上,称量,计算所得精盐的产率。
【实验分析】
(1)步骤①中因为,导致实验后精盐产率比其他同学偏低。
(2)步骤③中出现的错误操作是
该操作中玻璃棒的作用
A.加快蒸发速率 B.防止因局部温度过高,造成液滴飞溅 C.引流
【实验反思】经过这样操作所得到的精盐是纯净物吗?
【查阅教材】粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。
【实验设计】
| 实验操作 |
预计实验现象 |
实验结论及解释 |
| ①将少量所得精盐溶于水,滴加少量稀NaOH溶液 |
所得精盐中可能含有氯化镁 化学方程式 |
|
| ②取实验①中的上层清液继续滴加NaOH溶液至不再有沉淀时,在上层清液中再滴加 溶液 |
出现白色沉淀 |
所得精盐中可能含有氯化钙 化学方程式 |
【实验结论】除去难溶性杂质得到的精盐不是纯净物。
下图是关于探究燃烧条件的三个实验装置。
(1)写出白磷燃烧的化学方程式;
(2)与甲图装置相比,乙图装置的优点是:;
有同学提出乙图装置仍然有不足之处,请你设计实验进行改进。 用文字描述或画出实验装置图。
。
(3)丙图装置中木屑燃烧,煤粉没有燃烧,说明燃烧的条件之一是。
母亲节前夕,阳阳对妈妈给外婆购买的“XX牌”苏打饼干及其配料表产生了浓厚的兴趣。在化学课上,阳阳听老师说过,苏打是碳酸钠(Na2CO3)的一个俗名,她再仔细阅读该饼干的配料表如下:小麦粉、小苏打……。她思考:配料中小苏打有何作用?如何鉴别苏打(Na2CO3)和小苏打(NaHCO3)?……
下面是阳阳进行的研究性学习过程,请你参与并回答相关问题。
【资料获悉】
1.相同条件下,Na2CO3溶液比NaHCO3溶液的碱性强;
2.20℃时,Na2CO3、NaHCO3的溶解度分别为21.3g和9.6g;
3.NaHCO3在2700C时能发生如下分解反应:2NaHCO3加热Na2CO3+H2O+CO2↑
而Na2CO3受热不易分解。
【实验过程】
实验一:验证Na2CO3和NaHCO3热稳定性的差异。在老师的指导下,你们按题18图所示进行实验若实验现象为,则能得出NaHCO3受热易分解,Na2CO3受热不易分解。
实验二:用酸碱度的差异鉴别Na2CO3和NaHCO3。你们若用广泛pH试纸测定相同条件下两种溶液的pH,则pH较大的是。
实验三:用20℃时溶解度的差异鉴别Na2CO3和NaHCO3
请完成下表:(忽略溶解过程中热量的变化)
| 实验操作 |
预期的现象和结论 |
| (3) |
(4) |
【交流总结】
1.配料中小苏打主要起发泡作用。
2.可以通过溶解度、酸碱度等差异来鉴别Na2CO3和NaHCO3。
【拓展延伸】
通过上述研究性学习过程。你们认为小苏打(NaHCO3)除用于食品工业外,在日常生活及实验室中还有哪些应用,试举一例:。