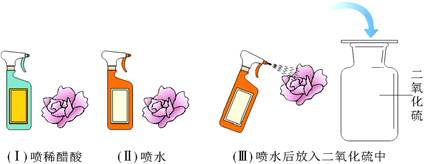
(2013湖北宜昌)二氧化硫是造成酸雨的主要物质之一。小丽为探究二氧化硫能与水反应生成酸,设计了如下实验方案。
【实验设计】她先用紫色石蕊溶液将白色滤纸浸润,干燥后做成紫色的小花,然后按下列图示进行实验。观察到实验(Ⅰ)和(Ⅲ)中的小花变红,(Ⅱ)中的小花不变色。
【评价反思】小虎对小丽的实验方案提出了质疑,他认为上述实验还不足以证明“二氧化硫和水反应生成了酸”。两位同学仔细讨论后认为还需补充如下一个实验,才能得出二氧化硫与水反应生成酸。
| 实验操作 |
实验现象 |
| |
|
【拓展应用】二氧化硫也是实验室一种污染气体,常用碱液吸收。写出实验室用氢氧化钠溶液吸收二氧化硫的化学方程式: 。
根据如图实验装置,回答问题:

(1)C装置中标有①的仪器名称为 。
(2)实验室某小组同学用过氧化氢溶液和二氧化锰制取氧气,请写出化学方程式 ;根据该反应原理,从控制反应速率的角度考虑,请从如图中选择发生装置和收集装置制取一瓶干燥的氧气,所选装置接口字母连接顺序为 (连接顺序全对才得分)。
如图是中学化学实验中常用的一些装置,请回答下列问题:

(1)写出标注仪器的名称:① ,② 。
(2)实验室用双氧水和二氧化锰制取氧气时应选用 (填字母序号,下同)作发生装置,反应的化学方程式为 ;若要收集较为纯净的氧气最好选用 装置。
(3)①实验室用B装置制取 时,装入块状石灰石的操作方法是 ;
②收集 不选用C装置的理由是 。
(4)通常情况下氯气是一种黄绿色有刺激性气味的气体,密度比空气大。实验室用固体高锰酸钾和浓盐酸反应制取氯气,若用F装置收集氯气,则气体应从图中的 (选填a或b)端进入,收集到的氯气中含有的杂质气体是 。
化学是一门以实验为基础的学科。根据如图装置回答问题:

(1)仪器X的名称是 。
(2)实验室用A装置可以制备 气体,反应的化学方程式为 。要除去制得的 气体中混有的杂质,可用饱和 溶液洗气,发生反应的化学方程式为 。
(3)实验室用A、B装置组合制取 。A装置中发生反应的化学方程式为 ,在该反应中 的质量和 在反应前后保持不变。若要对B装置收集的 验满,带火星的木条应置于 端(填“b”或“c”)。
(4)实验室要制取干燥的H2,装置接口的连接顺序为a→ → → 。电解水也可制得H2,装置如图D,收集到氢气的试管是 (填“f”或“g”)。
农场需用熟石灰改良酸性土壤,为了确保改良效果,需要对库存的熟石灰是否变质进行检测。农场实验室取了一定量的熟石灰样品,对其成分进行如下探究。
【提出问题】熟石灰样品的成分是什么?
【作出猜想】猜想一:
猜想二: 和
猜想三:
【资料查阅】氢氧化钙微溶于水
【实验步骤与现象】
|
步骤 |
操作 |
现象 |
|
1 |
取1g样品于试管中,加入10mL蒸馏水充分振荡 |
得到上层清液和下层固体 |
|
2 |
向步骤1后的试管中滴加几滴酚酞 |
溶液变红 |
|
3 |
向步骤2后的试管中逐滴滴加稀盐酸 |
溶液由红色变为无色,固体物质消失并产生气泡 |
【实验分析】
(1)实验人员根据步骤1认为猜想三正确。其实该结论并不严密,请说明理由 。
(2)解释步骤3有气泡产生的原因(用化学方程式表示) 。
【实验结论】通过以上实验可以知道猜想 正确。
【评价与反思】熟石灰存放时应密封保存。农业上使用库存较久的熟石灰时要检测其成分。
化学兴趣班的同学准备分组进行气体的制取与性质的探究实验,实验员准备了如图仪器,同学们根据所学知识完成下列题目。
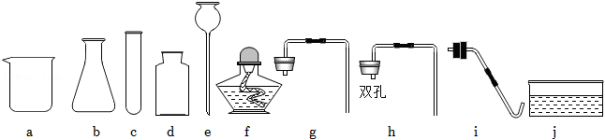
(1)请写出如图中对应字母编号为“e”的仪器名称 。
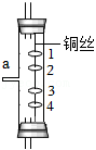
(2)甲小组的同学准备利用过氧化氢溶液制得较多量的氧气,同时便于添加液体试剂,应选择如图中的 (选填字母编号)来组成发生装置,生成氧气的化学方程式为 。
(3)乙小组的同学利用甲小组组装的发生装置制得了二氧化碳气体,并将气体从如图a端通入以探究二氧化碳的性质,其中1、4为湿润的石蕊棉球,2、3为干燥的石蕊棉球。同学们观察到2、3棉球不变色,1、4棉球变红且4棉球先变红,根据实验现象可得出二氧化碳的物理性质是 ,二氧化碳的化学性质是(用化学方程式表示) 。