高纯氧化钙是用于电子工业重要的无机化工原料.用硝酸钙溶液制备高纯氧化钙的工艺流程如下:
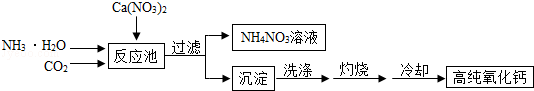
反应池中发生反应的化学方程式为:CO3+2NH3•H2O+Ca(NO3)2═2NH4NO3+CaCO3↓+H2O
请回答下列问题:
(1)过滤操作中玻璃棒的作用是 .
(2)过滤后所得沉淀表面可能含有的可溶性杂质有 (写出一种即可).
(3)该工艺流程中可循环使用的物质是 .
(4)冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有的杂质是 .
(5)上述流程中的副产物NH4NO3可用作氮肥,氮肥的主要作用是 .
A、促进植物生长,叶色浓绿
B、增强作物的抗寒,抗旱能力
C、增强作物的抗病虫害和抗倒伏能力.
实验探究和证据推理是提升认知的重要手段。化学兴趣小组对"CO还原Fe 2O 3粉末"的实验进行探究:
Ⅰ探究CO与Fe 2O 3的反应产物(夹持仪器已略去)
【实验过程】步骤1 在通风橱中,按图Ⅰ连接装置并检验装置的气密性。
步骤2 装入试剂:玻璃管内装入Fe 2O 3粉末,试管Ⅰ中装入澄清石灰水。
步骤3 从a端通入CO一段时间,待 ,再点燃酒精灯。
【实验现象】反应一段时间后,玻璃管内粉末由 色变成黑色,生成的黑色固体均能被玻璃管上方的磁铁吸引。试管Ⅰ中出现白色沉淀(用化学反应方程式表示: )。
【查阅资料】铁粉、FeO、Fe 3O 4均为黑色固体;铁粉、Fe 3O 4均能被磁铁吸引。
【提出猜想】对磁铁吸引的黑色固体成分有以下三种猜想:
猜测Ⅰ:Fe; 猜测Ⅱ:Fe 3O 4; 猜测Ⅲ:Fe和Fe 3O 4
【实验验证】取少量反应后的黑色固体放入试管中,加入足量的硫酸铜溶液,振荡,充分反应后静置,观察到红色固体中混有黑色颗粒,说明 (填"猜想Ⅰ""猜想Ⅱ"或"猜想Ⅲ")是正确的。
【拓展研究】进一步查阅资料,发现CO能溶于铜液[醋酸二氨合铜(Ⅰ)和氨水的混合液].因此可在装置Ⅰ后再连接下图装置Ⅱ,其目的是 ,装置Ⅰ、Ⅱ的连接顺序:b连接 (填"c"或"d")。

Ⅱ原料气CO的制备
方法一:加热MgCO 3、Zn的混合物可快速制备CO,同时还得到两种金属氧化物: 、 (填化学式)。
方法二:加热草酸晶体(H 2C 2O 4•2H 2O)制备CO:
H 2C 2O 4•2H 2O  CO↑+CO 2↑+3H 2O
CO↑+CO 2↑+3H 2O
已知:常压下,草酸晶体的熔点为101℃.比较草酸晶体的熔点和分解温度,分析若选用图装置Ⅲ制备装置Ⅰ所需的CO,可能存在的问题是 。
兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究。
【提出问题】它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
【实验探究1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
|
液体名称 |
蒸馏水 |
碳酸氢钠溶液 |
碳酸钠溶液 |
氢氧化钠溶液 |
|
紫甘蓝汁液显示的颜色 |
蓝紫色 |
蓝色 |
绿色 |
黄色 |
查阅资料:
|
pH |
7.5~9 |
10~11.9 |
12~14 |
|
紫甘蓝汁液显示的颜色 |
蓝色 |
绿色 |
黄色 |
【得出结论1】三种溶液的碱性由强到弱的顺序为 。
【实验探究2】甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由 色变为 色。向其中加入稀盐酸,该反应的化学方程式为 。
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图1所示。a点表示的意义是: 。
【得出结论2】从微观角度分析,该反应的实质是 。
【实验探究3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图2、图3所示。

【交流与反思】b点的溶质为 (写化学式),将图2和图3的阴影部分进行叠加,发现两者基本重合,c点的溶质 (写化学式)
【得出结论3】通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示: 、 。
【结论与反思】探究溶液的酸碱性及反应pH值的变化,可以认识反应的原理及进行的过程。
氯化镁是一种重要的化工原料,同学们在实验室对其开展了系列研究.
课题1:选择制取氯化镁的原料
【查阅资料】
①全球海水中含有的盐类总质量为5亿吨,其中含有的各种离子占盐类总质量的百分含量如下表所示:
|
离子 |
Cl﹣ |
Na+ |
Mg2+ |
Ca2+ |
K+ |
其他 |
|
含量 |
55.06% |
30.61% |
3.69% |
1.15% |
1.10% |
… |
②工业生产中海水或卤水(海水晒盐后的剩余溶液)都可以作为制取氯化镁的原料.
【交流讨论】
同学们经讨论,一致选择卤水用于实验室制取氯化镁.你认为他们的理由是
.
课题2:由卤水制取氯化镁
同学们设计如图所示方案,从卤水中制取氯化镁.
(1)溶液X的名称是 .
(2)部分同学认为上述制取方案不够完善,在“过滤”操作后缺少“洗涤”操作,从而导致制取的氯化镁不纯,可能混有的杂质是 .
课题3:测定氯化镁产品的纯度(氯化镁的质量分数)
同学们设计如下实验方案对制得的氯化镁进行纯度测定.
【实验步骤】
①称取9.5g氯化镁样品,放于烧杯中,加足量的水溶解,形成溶液;
②向上述溶液中加入90g质量分数为10%的氢氧化钠溶液;
③充分反应后,过滤;
④…
⑤向所得溶液中加入几滴无色酚酞试液,溶液变红,再逐滴加入10%稀硫酸(密度为1.07g•mL﹣1),并 ,当观察到溶液恰好褪色且30s内红色不复现,停止加入稀硫酸;
⑥计算氯化镁样品的纯度.
【问题讨论】
(1)为计算出氯化镁样品的纯度,除上述数据外,实验还需测量的数据是 .
(2)若缺少步骤④,则会导致氯化镁纯度测定不准确,步骤④的操作是 .
小文同学利用长柄W形玻璃管,完成了课本上多个化学实验.
(1)燃烧条件的探究与空气中氧气含量的粗略测定
①燃烧条件的探究:在如图1所示装置(省略夹持仪器,下同)中,向W形玻璃管中放入足量红磷和白磷,塞好橡皮塞,关闭活塞,然后将其放入80℃的热水中,观察到红磷不燃烧而白磷燃烧,说明可燃物发生燃烧应具备的条件是 .
②空气中氧气含量的粗略测定:为减小测量误差,待火焰熄灭后,将玻璃管 ,再打开活塞.
(2)一氧化碳与氧化铁反应

①甲酸(HCOOH)在热浓硫酸的作用下,分解生成一氧化碳和水,该反应的化学方程式是 .
②实验时,A处可以观察到的现象是 .
(3)探究微粒的性质
向玻璃管左端加入试剂X,观察到无色酚酞试液变红,湿润的红色石蕊试纸变蓝,试剂X可能是 ,该装置的优点有 (答1点).
根据如图回答下列问题:

(1)图B中标有序号①的仪器名称是 .
(2)组装好气体发生装置后,先应该检查装置的 ,然后再添加药品.
(3)欲收集密度比空气大的气体,应该选择的装置是 (填序号).
(4)实验室用石灰石与稀盐酸反应制取二氧化碳的化学方程式是 .