液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如下图装置①。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列有关叙述不正确的是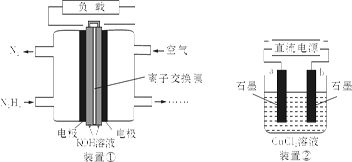
| A.该燃料电池负极发生的电极反应为:N2H4+4OH-−4e-==N2↑+4H2O |
| B.用该燃料电池作为装置②的直流电源,产生7.1g Cl2至少需加入0.5 mol N2H4 |
| C.该燃料电池中,电子从左侧电极经外电路流向右侧电极,溶液OH-迁移到左侧 |
| D.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.常温常压下,22.4 L乙烯中含C-H键的数目为4NA |
| B.1molFe与足量盐酸反应转移电子数为3NA |
| C.1.6g由氧气和臭氧组成的混合物中含有的氧原子数目为0.1NA |
| D.向1L 1mol·L—1氯化铝溶液中加入足量的氨水,生成AlO2-的个数为NA |
下列反应的离子方程式书写正确的是
| A.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| B.稀 HNO3与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C.氢氧化钡溶液与稀H2SO4反应:Ba2++ OH-+ H+ +SO42-=BaSO4↓+H2O |
| D.碳酸钙与醋酸反应:CO32-+2H+=H2O+CO2↑ |
下列反应或过程中能量的变化如右图所示的是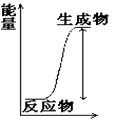
| A.H + H → H—H |
B.2NH4Cl + Ba(OH)2·8H2O BaCl2+2NH3↑+10H2O BaCl2+2NH3↑+10H2O |
C.Mg + 2HCl MgCl2 + H2 ↑ MgCl2 + H2 ↑ |
D.H2SO4 + 2KOH K2SO4 + 2H2O K2SO4 + 2H2O |
下列关于苯的说法中,不正确的是
A.苯不溶于水,可以作为萃取剂将溴从水中分离出来
B.分子中含有三个C-C键和三个C=C键
C.分子中C、H元素的质量比为12:1
D.在空气中燃烧时产生浓烟
在强酸性或强碱性溶液中都能大量共存的一组离子是
| A.Ba2+、Fe3+、Cl-、NO3- | B.Na+、Ca2+、HCO3-、NO3- |
| C.Al3+、NH4+、SO42-、Na+ | D.Na+、K+、NO3-、SO42- |