实验小组研究碳酸钠和碳酸氢钠的性质。
实验一:甲、乙、丙三位同学分别用溶质质量分数为5%的NaHCO3溶液和Na2CO3溶液进行了如下实验。
| 实验内容 |
NaHCO3溶液 |
Na2CO3溶液 |
| (1)加入无色酚酞溶液 |
溶液变红 |
溶液变红 |
| (2)加入澄清石灰水 |
产生白色沉淀 |
现象Ⅰ |
| (3)加入5%的CaCl2溶液 |
产生白色沉淀、有气泡产生 |
产生白色沉淀 |
| (4)加入稀盐酸 |
现象Ⅱ |
有气泡产生 |
| (5)加热溶液,并用导管与澄清石灰水连接 |
石灰水变浑浊 |
石灰水无明显变化 |
(1)表中的现象Ⅰ为 ;用化学方程式表示现象Ⅱ的原因 。
(2)若要鉴别实验中用到的NaHCO3和Na2CO3两种溶液,实验一中提供了 种方法。
实验二:甲、乙、丙三位同学分别将各自实验一中NaHCO3溶液与澄清石灰水反应后的物质进行过滤,对滤液中的溶质成分进行了如下探究。
【查阅资料】
(1)氯化钙溶液显中性,与氢氧化钠溶液不反应。
(2)两种溶液的取用量不同,滤液中溶质的组成情况可能有:①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④Na2CO3和NaHCO3;⑤Na2CO3和NaOH。
【进行实验】
| |
实验操作 |
实验现象 |
实验结论 |
| 甲同学 |
取少量滤液于试管中,滴加足量的稀盐酸 |
有气泡产生 |
滤液中的溶质一定含有Na2CO3 |
| 乙同学 |
取少量滤液于试管中,向其中通入少量CO2 |
产生白色沉淀 |
则滤液中的溶质是 |
| 丙同学 |
取少量滤液于试管中,塞紧胶塞,并用导管与澄清石灰水连接,加热 |
澄清石灰水变浑浊 |
则滤液中的溶质是Na2CO3和NaHCO3 |
【反思与评价】
(1)根据丙同学的结论,NaHCO3溶液与澄清石灰水反应的化学方程式是 。
(2)甲同学进一步实验,确定了滤液中的溶质是Na2CO3和NaOH。其实验方案是 。
实验是实现科学探究的重要途径。请回答以下有关问题: 
(1)仪器②的名称是_____________。
(2)用上图仪器组装成气体发生装置,该装置既可制取氢气又可制取氧气,应选(填序号)。写出实验室制取氧气的化学方程式。
(3)实验室制取二氧化碳,E装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是,若不加油层会使测定结果(填“偏大”或“偏小”)。
化学是一门实验科学,关注物质变化过程,探究物质变化的条件很有必要。某化学兴趣小组做了如下图所示的实验。
A.探究燃烧的条件 B.探究铁钉生锈的条件
根据上述实验,回答下列问题:
(1)实验A 是通过控制哪些因素来探究可燃物燃烧的条件?
(2)写出白磷燃烧的化学方程式
(3)实验B中,中间试管的实验目的是什么?
(4)请总结出铁制品发生锈蚀的主要条件
(5)写出防止铁制品锈蚀的一种方法。
下图所示为实验室中常见的气体制备和收集装置。请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用发生装置(填字母序号),反应的化学方程式为。若用装置
收集氧气,验满的方法是。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用
的优点是。
(3)欲使用装置
用排空气法收集二氧化碳,则气体应从(填"
"或"
")端通入;欲使用装置
用排水法收集氧气,先将瓶中装满水,再将气体从(填"
"或"
")端通入。
(4)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置(填字母序号)。
在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,某小组同学按图所示流程进行实验,请你参与讨论并回答相关问题.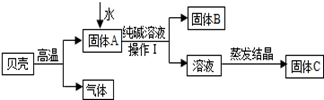
Ⅰ.定性研究
(1)生成固体B的化学反应方程式______________________________________________;
(2)操作Ⅰ指的是______________,其中要用到的玻璃仪器有烧杯、玻璃棒、;
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是__________________。
【猜想与假设】小组同学根据实验流程对所得的固体C的组成提出了质疑:甲同学认为:可能是NaOH、Na2CO3;乙同学认为:可能是;丙同学认为:可能是NaOH
【交流与评价】请你把乙同学的可能猜想结果写在横线上;
【活动与探究】甲同学取原溶液向其中倾倒一定量的稀盐酸观察到有大量气泡产生,于是得出该溶液中的溶质是NaOH、Na2CO3的结论,证实了自己的猜想。
乙同学取原溶液向其中加入Na2CO3溶液无现象,据此否定了自己的猜想;他又重新取原溶液,向其中加入____________观察到与甲同学不同的现象,得出了和甲同学相同的结论。
丙同学为了验证上述结论也取原溶液向其中滴加了少量稀盐酸,却发现无气泡产生。
【解释与结论】大家经过分析找出了丙同学所用试剂与甲同学相同,却没有看到气泡的原因。你认为可能的原因是 。经过上述三位同学的共同努力,大家终于对溶液中溶质的成分得出了正确结论。
Ⅱ.定量探究
【提出问题】固体产品C氢氧化钠的质量分数是多少呢?
【设计实验】小组同学设计了两套不同的方案进行实验并测得数据如下: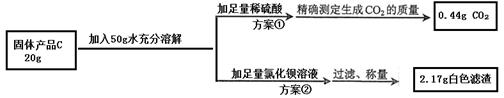
请你利用方案①所得数据计算固体产品C中氢氧化钠的质量分数(请列出计算过程)
【实验反思】
另一组同学根据方案②所得数据计算出的氢氧化钠质量分数与方案①相比明显偏小,请你分析其中的可能原因:_________________________________。
通过对化学的学习,你已掌握了实验室制取气体的有关规律,请结合下图回答有关问题:
(1)写出图中编号仪器的名称:①长颈漏;水槽
(2)选用A或B装置都能制备某种气体,用A装置制取该气体的化学反应方程式是:
,若选用G装置收集该气体,发生装置应与_______导管相连;
(3)实验室制取氢气时发生反应的化学方程式为_______________________________,若要制得干燥的氢气,可选用的装置组合是 F、C
(填编号),若选用C装置来制备该气体,反应进行过程中,关闭该装置中的弹簧夹后,可以观察到的现象是 ;
(4)某课外小组的同学收集到了含CO和CO2的废气,经过讨论认为废气中的CO可以利用,于是设计如下装置除去废气中的CO2,并收集一瓶CO,准备进行后续探究。你认为最合理的装置是___________________(瓶中盛放的是氢氧化钠浓溶液);