如图表示元素周期表前四周期的一部分,关于元素X、Y、Z、W的叙述正确的是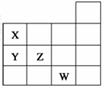
①X、Y的氧化物对应的水化物的酸性为Y<X
②W的原子序数比Z的大9
③W的单质常温下呈液态,可与铁粉反应
④Y、Z的气态氢化物的稳定性Y<Z
| A.①③ | B.①② | C.②③ | D.③④ |
如图为某有机物的结构简式,每个节点处代表有一个碳原子,与其结合的氢原子的元素符号省略,这种化学式称为“键线式”。又知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢化过程中不变,其反应原理如下:
关于该化合物的下列说法中,正确的是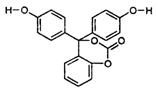
| A.该有机物的化学式为C20H14O5 |
| B.1mol该有机物与浓溴水反应,消耗5molBr2 |
| C.与足量氢氧化钠溶液充分反应,所得产物中相对分子质量较小的钠盐为HCOONa |
| D.1mol该有机物在铜铬氧化物催化下能与2mol氢气发生反应 |
将一定体积的CO2通入V L NaOH溶液中,已知NaOH完全反应,若在反应后的溶液中加入足量石灰水,得到Ag沉淀;若在反应后的溶液中加入足量CaCl2溶液,得到Bg沉淀,则下列说法正确的是
A.标准状况下,参加反应的CO2体积为0.224AL
B.用上述数据不能确定NaOH溶液的物质的量浓度
C.若A=B,则CO2与NaOH溶液反应的产物只有Na2CO3
D.B可能等于A、小于A或大于A
下列各组离子,在所给条件下一定能够大量共存的是
| A.pH=0的溶液中:Fe3+、Mg2+、NO3-、SO42- |
| B.能和Ca2+生成沉淀的溶液中:K+、Ba2+、CH3COO-、Cl- |
| C.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2—、SO32— |
| D.由水电离出的c(OH-)=1×10-13mol/L的溶液中:NH4+、Al3+、NO3-、Cl- |
下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是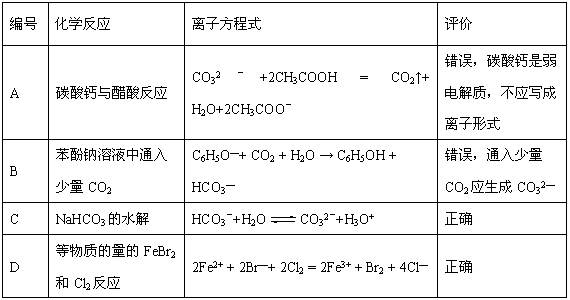
下列实验过程中产生的现象与对应的图形符合的是
| A.盐酸中加入NaAlO2溶液 | B.SO2气体通入溴水中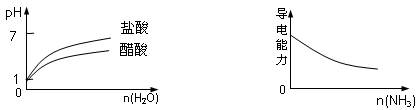 |
| C.pH=1的醋酸与盐酸分别加水稀释 | D.氨气通入醋酸溶液中 |