氨在国防、工农业等领域发挥着重要作用。
(1)工业以甲烷为原料生产氨气的过程如下:
①过程Ⅰ中,有关化学反应的能量变化如下图所示
反应①为 反应(填“吸热”或“放热”),CH4 (g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式是 。
②CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ)溶液吸收,其反应原理为: ,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是 。(选填字母)。
,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是 。(选填字母)。
a.高温、高压 b.高温、低压
c.低温、低压 d.低温、高压
③下表是过程Ⅱ中,反应物的量相同时,不同条件下平衡体系中氨的体积分数
Ⅰ.根据表中数据,得出的结论是 。
Ⅱ.恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡时n(N2)= 0.1mol,
n(H2)= 0.3mol。下列图象能正确表示该过程中相关量的变化的是 。(选填字母)。
(2)直接供氨式固体氧化物燃料电池能量转化率达85%,其结构示意图如图所示:
①负极的电极反应式是______。
②用该电池电解300ml的饱和食盐水。一段时间后,溶液pH=13(忽略溶液体积的变化),则消耗NH3溶液的体积是_____L。(标准状况)
氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解。请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。
 (1)某同学提出的假设是;
(1)某同学提出的假设是; (2)通过实验Ⅰ可以证明;
(2)通过实验Ⅰ可以证明; (3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步所做的确认为:在Ⅲ中先加入,再加入。
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步所做的确认为:在Ⅲ中先加入,再加入。 (4)探究结果为。
(4)探究结果为。 (5)你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是。
(5)你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是。
根据下图所示实验回答下列问题:
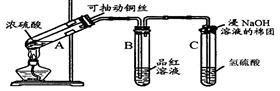
 (1)试管C口部的棉团上发生反应的离子方程式是。
(1)试管C口部的棉团上发生反应的离子方程式是。 (2)试管B中的实验现象是,若将该试管中反应后的溶液加热,可以观察到。试管C中溶液变浑浊,则证明SO2具有性。
(2)试管B中的实验现象是,若将该试管中反应后的溶液加热,可以观察到。试管C中溶液变浑浊,则证明SO2具有性。 (3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是,如果浸NaHCO3溶液,则发生反应的化学方程式是。
(3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是,如果浸NaHCO3溶液,则发生反应的化学方程式是。
某学习小组对教材实验“在200mL烧杯中放人20 g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15 mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究。




 (1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味。压缩“黑色面包”时,感觉较硬,放在水中呈漂浮状态。
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味。压缩“黑色面包”时,感觉较硬,放在水中呈漂浮状态。 同学们由上述现象推测出下列结论:
同学们由上述现象推测出下列结论: ①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③蔗糖炭化得到的碳连成整体,碳原子间形成了化学键 ④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③蔗糖炭化得到的碳连成整体,碳原子间形成了化学键 ④浓硫酸具有酸性 ⑤黑色物质具有强吸附性 其中依据不充分的是(填序号);
其中依据不充分的是(填序号); (2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:
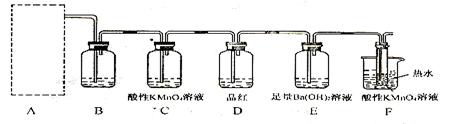
 试回答下列问题:
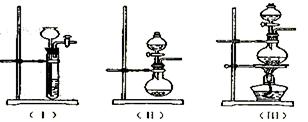
试回答下列问题: ①上图A中应选用下列装置(填编号)。
①上图A中应选用下列装置(填编号)。
 ②B装置所装试剂是;D装置中试剂的作用是
②B装置所装试剂是;D装置中试剂的作用是 ;E装置中发生的现象是;
;E装置中发生的现象是; ③A装置中使蔗糖变黑的化学反应方程式为;
③A装置中使蔗糖变黑的化学反应方程式为; ④F装置中酸性高锰酸钾溶液颜色变浅的原因是
④F装置中酸性高锰酸钾溶液颜色变浅的原因是 ;其反应的离子方程式是。
;其反应的离子方程式是。
研究性学习小组进行SO2的制备及性质探究实验。 (1)根据反应Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2+H2O,制备SO2气体。
(1)根据反应Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2+H2O,制备SO2气体。 ①用下列简图,在答题卡的方框中画出制备并收集SO2的实验装置(含试剂)示意图。
①用下列简图,在答题卡的方框中画出制备并收集SO2的实验装置(含试剂)示意图。
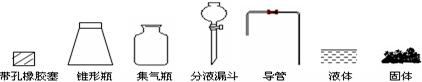
 ②实验过程中,使用分液漏斗滴加浓硫酸的操作是。
②实验过程中,使用分液漏斗滴加浓硫酸的操作是。 (2)将SO2气体分别通入下列溶液中:
(2)将SO2气体分别通入下列溶液中: ①品红溶液,现象是;
①品红溶液,现象是; ②溴水溶液,现象是;
②溴水溶液,现象是; ③硫化钠溶液,现象是。
③硫化钠溶液,现象是。 (3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。请你推测可能的原因并说明相应的验证方法(可以不填满)。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。请你推测可能的原因并说明相应的验证方法(可以不填满)。 ①原因,验证方法。
①原因,验证方法。 ②原因,验证方法。
②原因,验证方法。 ③原因,验证方法。
③原因,验证方法。
(1)将m g铁粉和n g硫粉均匀混合,在密闭容器中加热到红热,冷却后加入____Lb mol·L-1的盐酸就不再产生气体。若把已放出的气体收集起来,在标准状况下的体积是______。 (2)若把0.1 mol铁粉和1.6 g硫粉均匀混合后,铺在石棉网上用酒精灯加热引燃,完全反应后,将残渣全部放入过量的稀H2SO4中充分反应,结果所产生的气体体积在标准状况下明显少于2.24 L,其原因是__________________________________________________。
(2)若把0.1 mol铁粉和1.6 g硫粉均匀混合后,铺在石棉网上用酒精灯加热引燃,完全反应后,将残渣全部放入过量的稀H2SO4中充分反应,结果所产生的气体体积在标准状况下明显少于2.24 L,其原因是__________________________________________________。