【化学——选修3:物质结构与性质】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
| A |
578 |
1817 |
2745 |
11578 |
| B |
738 |
1451 |
7733 |
10540 |
A通常显____价,A的电负性______B的电负性(填“>”、“<”或“=”)。
(2)紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因___________;组成蛋白质的最简单的氨基酸中的碳原子杂化类型是 ;
| 共价键 |
C-C |
C-N |
C-S |
| 键能/ kJ·mol-1 |
347 |
305 |
259 |
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),已知3种离子晶体的晶格能数据如下表:
| 离子晶体 |
NaCl |
KCl |
CaO |
| 晶格能/kJ·mol-1 |
786 |
715 |
3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:_______________;其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有 个。
(4)[LiC60]PF6与NaCl具有类似的晶胞结构([LiC60]+表示1个Li+位于1个C60内部)。[LiC60]PF6晶体中包含的化学键有_____________(填字母);
A.金属键
B.离子键
C.极性键
D.非极性键
E.范德华力
已知[LiC60]PF6晶体晶胞边长为a nm,计算[LiC60]PF6晶体的密度为______g/cm3(用含a、NA的式子表示)。
(共18分)I写出下列热化学反应方程式
(1)N2 (g)与H2(g)反应生成1molNH3(g),放出46.1KJ热量。
(2)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8KJ热量。
(3)1molC(石墨)与适量H2O(g)反应吸收131.3KJ热量
II.(1)化学反应中均伴随着能量的变化,化学键的断裂和形成是发生能量变化的主要原因。生成物中化学键形成时会__________能量(填“放出”或“吸收”);如果一个化学反应,化学键断裂时的能量变化大于化学键形成时的能量变化,则该反应属于_________反应; 如果一个化学反应,反应物的总能量和生成物的总能量有如图所示的关系,则该反应属于__________反应。
如果一个化学反应,反应物的总能量和生成物的总能量有如图所示的关系,则该反应属于__________反应。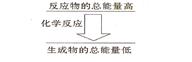
(2)不同形式的能量可以相互转换,如:化学能和电能、热能之间的相互转换。如图是一个原电池工作原理的示意图。试回答: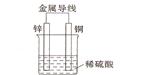
①从能量角度看,它属于____________能转化为____________能;
②装置中Zn为____________极。
(14分)硫酸工业中2SO2(g)+O2(g)催化剂△2SO3(g);ΔH<0(放热反应)有关实验数据如下:
  压强 压强SO2的 转化率 温度 |
1×105 Pa |
5×105 Pa |
10×105 Pa |
50×105 Pa |
100×105 Pa |
| 450 ℃ |
97.5% |
98.9% |
99.2% |
99.6% |
99.7% |
| 550 ℃ |
85.6% |
92.9% |
94.9% |
97.7% |
98.3% |
(1)在生产中常用过量 的空气是为了________。
的空气是为了________。
(2)高温对该反应有何影响?________,实际生产中采用400~500 ℃的温度除了考虑速率因素外,还考虑到________。
(3)增大压强对上述反应有何影响?____,但工业上又常采用常压进行反应,其原因是______________。
(4)常用浓H2SO4而不用水吸收SO3是由于___ ___,尾气中SO2必须回收,主要是为了________。
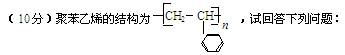
⑴聚苯乙烯的链节是,单体是。
⑵实验测得某聚苯乙烯的相对分子质量(平均值)为52 000,则该高聚物的聚合度n为。
⑶已知聚苯乙烯为线型结构的高分子化合物,试推测:溶于CHCl3,具有(填“热塑”或“热固”)性。
已知:A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题。
(1)D元素原子的结构示意图为( ) ;
(2)A、B、C三种元素的原子半径由小到大的顺序为( )(用元素符号表示);
(3)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为 ( ) ;
( ) ;
(4)A与D两元素的气态氢化物之间可以反应生成一种盐,该盐的水溶液呈( )(填“酸”、“碱”或“中”)性;
(5)实验室中,应将X的浓溶液保存在棕色试剂瓶中,其原因 是 ()
是 ()
(用化学方程式表示)。
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D、C与F分别为同一主族, A、D两元素的原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。B的氢化物的水溶液呈碱性。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
A、D两元素的原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。B的氢化物的水溶液呈碱性。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)A的元素符号是 ( ) F的元素符号是()B的氢化物的结构式 ( )
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的化学式为( ),其Y分子属于() (填“极性”、“非极性”)分子。
(3)一定条件下,A的单质气体与B的单质 气体充分反应生成6.8g W气体[已知反应的n(A):n(B)=3:1],可放出18.44 kJ热量,则该反应的热化学方程式( )
气体充分反应生成6.8g W气体[已知反应的n(A):n(B)=3:1],可放出18.44 kJ热量,则该反应的热化学方程式( )
(4)A的单质与C的单质与KOH溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入A的单质气体,N极通入C的单质气体,则N极的电极反应式( )。