[选修3—物质结构与性质]
19—Ⅰ下列物质的结构或性质与氢键无关的是 。
| A.乙醚的沸点 | B.乙醇在水中的溶解度 |
| C.氢化镁的晶格能 | D.DNA的双螺旋结构 |
19—Ⅱ钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。
回答下列问题:
(1)钒在元素周期表中的位置为 ,其价层电子排布图为 。
(2) 钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为 、 。
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是 对,分子的立体构型为 ;SO3气态为单分子,该分子中S原子的杂化轨道类型为 ;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为 ;该结构中S—O键长由两类,一类键长约140pm,另一类键长约为160pm,较短的键为 (填图2中字母),该分子中含有 个σ键。

(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为 ;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为 。
周期表中前20号几种元素,其相关信息如下(铍的原子半径为0.089nm):
| 元素代号 |
A |
B |
C |
D |
E |
| 原子半径/nm |
0.075 |
0.143 |
0.102 |
0.099 |
0.074 |
| 主要化合价 |
+5,—3 |
+3 |
+6,—2 |
—1 |
—2 |
F原子中无中子,G在地壳中含量居第二位,H元素焰色反应呈紫色。
请回答下列问题:
(1)B的原子结构示意图为。
(2)F2C和F2E两种化合物中,沸点较高的是(填化学式),原因是。
(3)用电子式表示化合物AF3的形成过程。
(4)G的单质能与H的最高价氧化物的水化物溶液反应,反应的化学方程式为。
(5)CE2能使酸性高锰酸钾溶液褪色(有Mn2+生成),写出其反应的离子方程式
。
(6)在2L密闭容器中,一定温度下,能说明反应2AE(g)+E2(g)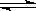 2AE2(g)已达到平衡状态的是(填代号)
2AE2(g)已达到平衡状态的是(填代号)
a. 2V逆(AE)=V正(E2)
b.容器内压强保持不变
c. 容器内密度保持不变
d. 各组分的物质的量浓度相等
e. 混合气体的平均相对分子质量不再改变
(7)某同学设计了以G同族的短周期元素的最低价氢化物为燃料的电池,电解质溶液含HEF。 则该电池的负极的电极反应式为。
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,Q、W、Z是非金属元素。五种元素核电荷数之和为55,对应原子最外层电子数之和为21。W、Z最外层电子数相同,但Z的核电荷数是W的2倍。
(1)Q在周期表中位于第周期族。
(2)X、Y各自的最高价氧化物对应的水化物可以发生反应生成盐和水,请写出该反应的离子方程式:。
(3)X单质能在W单质中燃烧可生成化合物R,R的电子式,该物质所含有的化学键的类型为 。
(4)Z的氢化物与W的氢化物发生反应生成Z单质和水,写出其化学方程式。
下表是元素周期表的一部分,表中所列字母分别代表一种元素。
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
| 一 |
A |
||||||
| 二 |
B |
C |
D |
E |
|||
| 三 |
F |
G |
H |
I |
K |
||
| 四 |
J |
L |
用合适的化学用语回答下列问题:
(1)上述元素中非金属性最强的是_____(填元素符号),J的氢氧化物的电子式:________。
(2)E、L两元素核电荷数之差是。
(3)某同学设计如下实验验证B、H非金属性的相对强弱。(酸性:H2SO3 >H2CO3)
①检查装置气密性,加药品后,打开a,然后滴入浓硫酸加热,铜与浓硫酸反应的化学方程式是。
②装置A中的试剂可以是。
a.Na2CO3溶液 b.溴水 c.酸性KMnO4溶液 d.NaOH溶液
③能说明碳的非金属性比硅强的实验现象是。
④若将第一支试管中试剂换为H2S溶液,试管中有浅黄色浑浊出现,该反应的化学方程式是 ;若换成新制氯水,则反应的离子方程式为。
(1)在CH4、H2S、NH4+、H2O、OH—、HCl、Na、Mg2+八种粒子中,选择符合下列要求的粒子填空:
①上述粒子中与K+质子数不同,电子数相同的有;
②上述粒子中与NH3质子数相同,电子数也相同的有;
③上述粒子中电子数大于质子数的有。
(2)用锌片、铜片和稀硫酸组成的原电池,该电池的负极材料是,正极的电极反应式为,电池工作时电子流向(填“正极”或“负极”)。
(3)将6molA气体和2molB气体在2L密闭容器中混合并在一定条件下发生反应:3A(g)+B(g) xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L•min),请填写下列空白:
xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L•min),请填写下列空白:
①x的数值为;
②A的平均反应速率为;
③5min时B的转化率为。
某有机物含有C、H、O三种元素,其质谱如图所示。将4.3 g该有机物在O2中充分燃烧,使生成物依次通过足量浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重8.8 g,则:
(1)该有机物的摩尔质量为____________g/mol。
(2)该有机物的分子式为。
(3)1mol该有机物与足量的金属钠反应产生1mol氢气,核磁共振氢谱有两个峰,且面积比为2∶1,请写出其结构简式。