(本题共12分)磷矿石的主要成分是Ca5F(PO4)3,并含有少量MgO、Fe2O3等杂质。工业上以磷矿石为原料制备H3PO4,一种生产流程如下: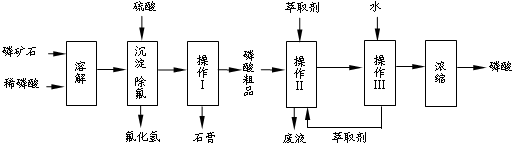
已知:Ca5F(PO4)3 + 7H3PO4→5Ca(H2PO4)2 + HF
38、写出有关操作的名称:Ⅰ___________、Ⅲ 。工艺流程中设计操作Ⅱ与Ⅲ的目的是 。
39、若在实验室里采用此种方法溶解磷矿石,请写出必须的实验注意事项,并说明理由: 。
40、磷矿石也可直接用硫酸溶解,两种工艺相比,该工艺的优点是____________________。
41、测定产品磷酸的浓度可采用滴定法。准确量取10.00 mL磷酸产品(密度为1.526g/cm3)溶于水配成1L溶液;取稀释后的溶液20.00mL,以甲基橙为指示剂,用0.103 mol/L标准NaOH溶液滴定;当观察到溶液恰好变色,且在半分钟内不变色,即为滴定终点(生成NaH2PO4),消耗标准溶液20.16 mL。
该实验过程中需要的定量仪器有______________________________(写名称)。
42、若理论上滴定应耗用标准溶液20.20 mL,则相对误差为______________(按近似计算法则)。该产品中磷酸的质量分数为 (保留3位小数)。
(14分)设计一个简单的一次性完成实验的装置图,目的是验证醋酸溶液,二氧化碳水溶液、苯酚溶液的酸性强弱顺序。
①利用上图所示的仪器可以组装实验装置,则仪器的连接顺序为:
接_____ , 接______ ,接(填字母)
②写出装置I和II中的实验现象:
I中;II中
③写出装置II中发生反应的方程式
④由强到弱排序三者的酸性顺序
某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。
(1)氯气可以用于漂白、消毒的原因是氯气能与水作用形成具有________性的次氯酸,相关反应的离子方程式为________________________;
(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8∶00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5 mg/L至1.0 mg/L 之间时,效果最好。上图是该小组测定的每天19∶00时游泳池中水的含氯量,有哪几天使用游泳池不卫生_________________:
(3)你认为哪几天的天气炎热、阳光强烈________,说出一种理由是____________ ____________;
(4)在对游泳池水中通入氯气消毒时,当发生氯气泄漏,应立即关闭氯气罐,还应采取下列自救方法________。(选填序号)
| A.用湿润的毛巾捂住口鼻跑向低处 |
| B.用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处 |
| C.用浸湿浓氨水的毛巾捂住口鼻匍匐跑至安全处 |
| D.用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处 |
(5)小型游泳池通常使用漂白液(NaClO溶液)而非氯气来消毒池水,试举出使用漂白液而非氯气消毒的一项理由________________________。
酯类是工业上重要的有机原料,具有广泛用途。
下图是乙酸乙酯的合成路线图,已知A能与银氨溶液反应析出银镜,B的水溶液可以溶解CaCO3,E可作果实催熟剂。
请完成下列问题:
(1)A的名称是________;B中所含的官能团是________;反应③的类型是;反应④的类型是。
(2)A的结构简式为________;E的结构简式为________。
(3)请写出反应③、④的化学方程式:③________;④________。
(4)请写出CH3COOCH2CH3的酯类物质的同分异构体的结构简式(写两种即可)。
Ⅰ.下列实验操作中正确的是
| A.分液时,分液漏斗下层液体从下端放出,上层液体从上口倒出 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.蒸发结晶时应将溶液直接蒸干 |
| D.称量非腐蚀性药品应放在托盘天平左盘的称量纸上,砝码放在托盘天平右盘的称量纸上 |
Ⅱ.影响化学反应速率的因素很多,某学校化学小组用实验的方法进行探究。他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来探究影响化学反应速率的因素。甲同学的实验报告如下表:
| 实验步骤 |
现象 |
结论 |
| ①分别取等体积2mol/L的硫酸于试管中 ② |
反应速率Mg>Fe,Cu反应最慢 |
金属性质越活泼,反应 速率越快 |
(1)甲同学表中实验步骤②为;
(2) 甲同学的实验目的是;要得出正确的实验结论,还需要控制的实验条件是。
乙同学为了更精确地研究浓度对反应速率的影响,利用右图所示装置进行定量实验。
(3)乙同学在实验中应该测定的数据是;
(4)乙同学完成实验应选用的实验药品是。
10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
| pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH值升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度(填“大于”或“小于”)NaHCO3。
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则(填“甲”或“乙”)判断正确。试剂X是。
A、Ba(OH)2溶液 B、BaCl2溶液 C、NaOH溶液 D、澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH(填“高于”、“低于”或“等于”)8.3,则(填“甲”或“乙”)判断正确。
(3)常温下,在测得PH都等于9的NaOH溶液和Na2CO3溶液中,由水电离的OH—浓度分别为amol /L和bmol /L,则a与b的关系:。