某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示: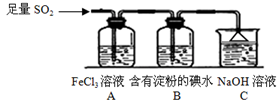
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在 中,再加水稀释,这样操作的目的是 。
(2)装置C的作用是 。
(3)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、 、自然干燥,在这一系列操作中没有用到的仪器有 (填序号)。
| A.蒸发皿 |
| B.石棉网 |
| C.漏斗 |
| D.烧杯 |
E.玻璃棒
F.坩埚
(4)根据以上现象,该小组同学认为SO2与 FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式 ;
②请设计实验方案检验有Fe2+生成 ;
③该小组同学向C烧杯反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法 (填“合理”或“不合理”),理由是 。
(5)能表明I-的还原性弱于SO2的现象是 。
已知硫酸亚铁铵晶体为浅绿色,易溶于水、不溶于乙醇,在水中的溶解度比FeSO 4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。以下是将绿矾(FeSO4•7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。
4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。以下是将绿矾(FeSO4•7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。
(已知: (NH4)2SO4+FeSO4+ 6H2O (NH4)2SO4•FeSO4•6H2O↓)根据下图回答:
(NH4)2SO4•FeSO4•6H2O↓)根据下图回答: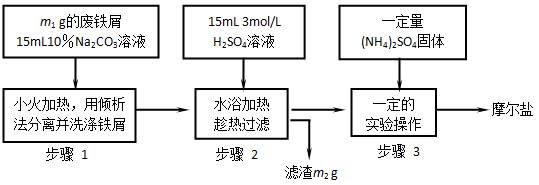
(1)步骤1中Na2CO3的主要作用是。
(2)步骤2中铁屑过量的目的是(用离子方程式表示):。步骤2中溶液趁热过滤的原因是。
(3)步骤3中,加入(NH4)2SO4固体后,应加热到溶液表 面出现晶膜时,停止加热。为什么不能蒸干?。需经过的实验操作包括:、 、减压过滤(或抽滤)等得到较为干燥
面出现晶膜时,停止加热。为什么不能蒸干?。需经过的实验操作包括:、 、减压过滤(或抽滤)等得到较为干燥
的晶体。步骤3中制得的晶体要用无水乙醇洗涤的目的是。
(4)摩尔盐产品中离子的检验:
甲同学提出可以用湿润的试纸、稀盐酸和溶液检验出这三种离子。
乙同学提出检验产品中的Fe2+,可以用KSCN溶液和另一种试剂来检验,试简述乙同学操作和现象:。
(5)产品中Fe2+的定量分析:
制得的摩尔盐样品中往往含有极少量的Fe3+。为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性下用KMnO4标准液滴定的方法。
称取4.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸。用0.2 mo1/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液体积10.00 mL。
①本实验的指示剂。
| A.酚酞 | B.甲基橙 | C.石蕊 | D.不需要 |
②KMnO4溶液置于(酸式、碱式)滴定管中
③产品中Fe2+的质量分数为。
配制0.5mol/L的NaOH溶液时,如果只存在下列问题,溶液的浓度如何变化?(填“偏高”、“偏低”、或“不变”)。
(1)称量NaOH固体时,天平的砝码粘有油污,其结果 ___________ 。
(2)向容量瓶中加蒸馏水超过了刻度线后,又用滴管把多出的部分吸走,其结果。
(3)观察刻度线时仰视,其结果 ___________。
(4)所用容量瓶中已有少量蒸馏水,其结果 _____________。
实验室可以用纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如下: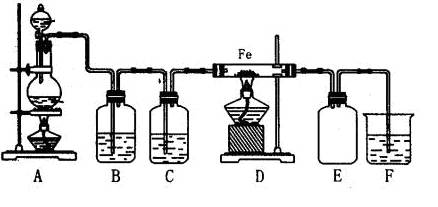
回答下列问题:
(1)A装置可制取氯气,反应前分液漏斗中药品为,圆底烧瓶中药品为。
(2)写出A装置中制取氯气所发生的化学方程式是。
(3)装置B中盛放的试剂是________________________。
(4)装置E的作用是______________________________。
某次实验需用0.4 mol·L-1 NaOH溶液480 mL。配制方法如下:
(1)配制该溶液应选用_______________mL容量瓶;
(2)用托盘天平准确称量__________g 固体NaOH;
(3)将称量好的NaOH固体放在500 mL大烧杯中,倒入约300 mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待__________________后,将烧杯中的溶液注入容量瓶中;
(4)用少量蒸馏水洗涤烧杯次,洗涤后的溶液___________________,轻轻晃动容量瓶,使溶液混合均匀;
(5)向容量瓶中加入蒸馏水,到液面________________________时,改用___________加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,_______________________________;
(6)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是___________,偏低的是___________,对实验结果没有影响的是___________(填各选项的序号)。
| A.所用的NaOH中混有少量Na2O |
| B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥 |
| C.配制溶液所用的容量瓶洗净后没有烘干 |
| D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作 |
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀 后静止,发现液面低于刻度线,再加蒸馏水至刻度线。
后静止,发现液面低于刻度线,再加蒸馏水至刻度线。
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。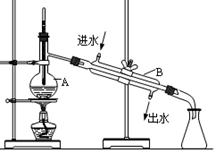
(1)图中的两处明显的错误是__________________ ;_______________________。
(2)A仪器的名称是____________,B仪器的名称是_______________。
(3)实验时A中除加入少量自来水外,还需加入少量_______,其作用是__________