芳香酯类化合物A、B互为同分异构体,均含C、H、O三种元素。相同状况下,A、B蒸气对氢气的相对密度是97,分子中C、H原子个数相同,且C、H原子数之和是O原子数的5倍。
(1)A的分子式是________________。已知:各有机物间存在如下转化关系
其中C能发生银镜反应,F经连续氧化可生成C;C与D是相对分子质量相同的不同类型的有机物。
(2)水杨酸中所含官能团的名称是____________;完全燃烧时,1 mol D与1 mol 下列有机物耗氧量相同的是____________(填字母代号)。
a.C3H6O3 b.C3H8O c.C2H4 d.C2H6O2
(3)B的结构简式是________________________;
水杨酸与小苏打溶液反应的化学方程式:___________________________;一定条件下,C与F反应的反应类型是____________。
(4)写出C与足量银氨溶液的反应化学方程式______________;反应类型是____________。
(5)同时符合下列要求的化合物有____________种。
①与A互为同分异构体
②可以水解
③苯环上有两个取代基,且苯环上的一氯代物只有1种
(6)1 mol上述(5)中的一种有机物X 在水溶液中,能与4 mol NaOH共热发生反应,写出此反应的化学方程式:____________________________________。
已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(金刚石、s)+O2(g)=CO2(g);△H=-395.41kJ/mol,C(石墨、s)+O2(g)=CO2(g);△H=-393.51kJ/mol,则金刚石转化石墨时的热化学方程式为:____________________________________。
由此看来更稳定的碳的同素异形体为:____________。若取金刚石和石墨混合晶体共1mol 在O2中完全燃烧,产生热量为QkJ,则金刚石和石墨的物质的量之比为_____________(用含Q的代数式表示)
镁、铝是两种重要的金属,它们的单质及化合物有着各自的性质。
Ⅰ.海水中含有氯化镁,是镁的重要来源之一。从海水中制取镁,某同学设计了如下
流程步骤:
主要的步骤总结如下:①把贝壳制成石灰乳②往母液中加石灰乳,沉降、过滤,得到Mg(OH)2沉淀③将沉淀物与盐酸反应,结晶、过滤,将制得的晶体脱水得无水MgCl2
④将得到的产物熔融后电解。
(1)下列说法不正确的是__________________(填代号)
| A.此法的优点之一是原料来源丰富 |
| B.进行①②③步骤的目的是从海水中提取氯化镁 |
| C.第④步电解法制取镁是由于镁是很活泼的金属 |
| D.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应 |
(2)步骤②不够合理,理由是
Ⅱ.(1)铝、空气、海水可组成一种电池,广泛用于制造航标灯。此电池正极的电极反应为。
(2)铝热还原法是冶炼熔点较高的金属的一种重要方法,焊接钢轨即用到此法。将干燥的氧化铁粉末和铝粉均匀混合后放入纸漏斗中(漏斗已事先处理好),并架在铁架台上,
下面放置一个盛有沙子的蒸发皿。请写出引发铝热反应的操作及该反应的化学方程式:
操作
化学方程式。
(3)为确定某铝热剂(氧化铁粉末和铝粉)的组成,分别进行下列实验。
若取10.7g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况)体积为3.36L,反应的化学方程式为,样品中铝的质量是g。
若取10.7g样品将其点燃,恰好完全反应,待反应产物冷却后,加入足量盐酸,测得生成的气体体积为aL,该气体与上小题中所得气体的体积比等于∶。
已知乙烯能发生以下转化关系:
试回答下列问题:
(1)乙烯的电子式为;B中含官能团名称是。
(2)写出反应的化学方程式
①,反应类型:;
②,反应类型:;
④,反应类型:。
(3)现拟分离含B、D和水的乙酸乙酯粗产品,下图是分离操作流程,请在图中圆括号内
填入适当的试剂,在方括号内填入适当的分离方法。
试剂a是__________,b是_______________;
分离方法①是__________,②是______________;
(4)与B和D在浓硫酸催化作用下发生反应相似,B的同系物X也能和D发生反应生成酯Y,Y的分子量比乙酸乙酯大28,则X的分子式为,X的结构简式为(写出一种即可)。
X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+3、+5、+7,核电荷数按照Z、X、Y、W的顺序增大。已知Z的原子次外层的电子数为2,W、X原子次外层电子数为8。
(1)请写出元素Y的原子结构示意图;其中元素W在周期表中的位置。
(2)用电子式表示X在空气中生成的氧化物的形成过程:。
(3)X、Y、Z、W的原子半径由大到小的顺序为:。(用元素符号表示)
(4)请写出W的单质与X的最高价氧化物对应水化物反应的离子方程式:。
(5)写出Z与氢元素形成的10电子微粒化学式(任写两种)。
(6)元素X与元素Y相比,金属性较强的是(用元素符号表示),请举一例实验事实证明这一结论。
21世纪最富有挑战性的课题之一是使汽油氧化直接产生电流,新研制的某汽油燃料电池的一个电极通入空气,另一个电极通入汽油蒸气,用NaOH溶液作电解质溶液。填写下列空格。
(1)汽油_____________(选填“有”或“没有” )固定的熔沸点。炼制汽油的原料是石油,工业上生产汽油的常用方法是。(填序号)
①分馏 ②干馏 ③裂化 ④聚合
(2)汽油中有一种烃的成分为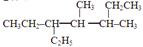 ,它的分子式是,名称是。
,它的分子式是,名称是。
(3)汽油燃料电池的能量转换形式是将能直接转化为能。通入空气的那个电极是燃料电池极(选填“正”或“负”)。若汽油的组成用上述烃的分子式表示,则负极的电极反应式为。