隔膜电解法处理高浓度乙醛废水的原理是使乙醛分别在两极发生反应,转化为乙醇和乙酸。实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如右图所示。有关说法不正确的是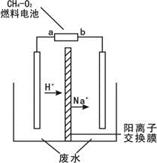
| A.图中燃料电池的a极应通入氧气 |
| B.乙醇在阴极产生 |
| C.电解过程中,阴极区有NaOH产生 |
| D.每生成1mol乙酸,理论上至少消耗标况下氧气22.4L |
下列生产、生活情境都涉及能量转化和利用,其中不发生化学变化的是
氢氧燃料电池是将H2和O2通入电池,穿过浸入20%—40%的KOH溶液的多孔碳电极,其电极反应式分别为:2H2+4OH--4e-= 4H2O和O2+2H2O+4e-= 4OH-,下列不正确的是
| A.氢氧燃料电池属于环境友好电池 |
| B.通O2的极是正极,通入H2的极是负极 |
| C.工作一段时间后KOH溶液的溶质质量分数增大 |
| D.工作时溶液中的OH-向负极作定向移动 |
下列反应的离子方程式中,书写正确的是
| A.氯气溶于水:H2O + C12=2H+ +ClO-+Cl- |
| B.将铝粉投入氢氧化钠溶液中:2Al+2OH-=2AlO2-+H2↑ |
| C.铁粉与氯化铁溶液反应:Fe + Fe3+=2Fe2+ |
| D.过氧化钠与水反应:2Na2O2+ 2H2O = 4Na+ + 4OH+ O2↑ |
在一定条件下,反应N2+3H2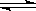 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为
| A.V(NH3)=0.02mol/(L·min) | B.V(N2)=0.005mol/(L·min) |
| C.V(NH3)=0.17mol/(L·min) | D.V(H2)=0.03mol/(L·min) |
关于基本营养物质的说法正确的是
A.糖类、油脂、蛋白质都是都是高分子化合物
B.葡萄糖和蔗糖都能发生水解反应
C.糖类、油脂、蛋白质都是由C、H、O三种元素组成的
D.油脂在酸性条件下水解为丙三醇和高级脂肪酸