物质的类别和核心元素的化合价是研究物质性质的两个重要视角。硫及其化合物与价态变化为坐标的二维转化关系如图所示。完成下列填空:
(1)图中X的水溶液在空气中放置易变浑浊,写出反应的化学方程式: ;
(2)下列物质用于Na2S2O3制备,从氧化还原反应的角度
分析,理论上有可能实现的方案是 (选填编号)。
a.Na2S + S b.Z + S c.Na2SO3 + Y d.NaHS + NaHSO3
(3)请补充完整焙烧明矾的化学方程式:
___KAl(SO4)2·12H2O +____S = ____K2SO4 + ____Al2O3 + ____SO2↑ +
(4)研究反应Na2S2O3 + H2SO4 ="=" Na2SO4 + S↓ + SO2↑+ H2O的速率时,下列方案合理的是 (选填编号)。
a.测定一段时间内生成SO2的体积,得出该反应的速率
b.研究浓度、温度等因素对该反应速率的影响,比较反应出现浑浊的时间
c.用Na2S2O3(s)分别与浓、稀硫酸反应,研究浓度对该反应速率的影响
(5)治理含CO、SO2的烟道气,以铝钒土做催化剂,将CO、SO2在380℃时转化为S 和一种无毒气体。已知:①硫的熔点:112.8℃、沸点:444.6℃;
②反应每得到1mol硫,放出270kJ的热量。写出该治理烟道气反应的热化学方程式 。
(6)其他条件相同、催化剂不同时,上述反应中SO2的转化率随反应温度的变化如图。不考虑催化剂价格因素,生产中选铝矾土做催化剂的主要原因是 。
2013年10月我市因台风菲特遭受到重大损失,市疾控中心紧急采购消毒药品,以满足灾后需要。复方过氧化氢消毒剂具有高效、环保、无刺激无残留,其主要成分H2O2是一种无色粘稠液体,请回答下列问题:
(1)下列方程中H2O2所体现的性质与其可以作为消毒剂完全一致的是。
A.BaO2+2HCl H2O2+BaCl2
H2O2+BaCl2
B.Ag2O+H2O2 =2Ag+O2+H2O
C.2H2O2 2H2O+O2↑
2H2O+O2↑
D.H2O2+NaCrO2+NaOH=Na2CrO4 +H2O
(2)火箭发射常以液态肼(N2H4)为燃料,液态H2O2为助燃剂。已知:
N2H4(1)+O2(g)=N2(g)+2H2O(g)△H=" -" 534 kJ·mol-1
H2O2(1)=H2O(1)+1/2O2(g)△H=" -" 98.64 kJ·mol-1
H2O(1)=H2O(g)△H=+44kJ·mol-l
则反应N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)的△H=,
该反应的△S=0(填“>”或“<”)。
(3)H2O2是一种不稳定易分解的物质。
①如图是H2O2在没有催化剂时反应进程与能量变化图,请在图上画出使用催化剂加快分解速率时能量与进程图
②实验证实,往Na2CO3溶液中加入H2O2也会有气泡产生。已知常温时H2CO3的电离常数分别为Kal=4.3×l0-7,Ka2 =" 5.0" ×l0-11 。Na2CO3溶液中CO32-第一步水解常数表达式Khl=,常温时Khl的值为。若在Na2CO3溶液中同时加入少量Na2CO3固体与适当升高溶液温度,则Khl的值
(填变大、变小、不变或不确定)。
(4)某文献报导了不同金属离子及其浓度对双氧水氧化降解海藻酸钠溶液反应速率的影响,实验结果如图1、图2所示。
注:以上实验均在温度为20℃、w(H2O2)=0.25%、pH=7.12、海藻酸钠溶液浓度为8mg·L-l的条件下进行。图1中曲线a:H2O2;b:H2O2+Cu2+;c:H2O2+Fe2+;d:H2O2+Zn2+;e:H2O2+Mn2+;图2中曲线f:反应时间为1h;g:反应时间为2h;两图中的纵坐标代表海藻酸钠溶液的粘度(海藻酸钠浓度与溶液粘度正相关)。
由上述信息可知,下列叙述错误的是(填序号)。
A.锰离子能使该降解反应速率减缓
B.亚铁离子对该降解反应的催化效率比铜离子低
C.海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢
D.一定条件下,铜离子浓度一定时,反应时间越长,海藻酸钠溶液浓度越小
有五种摩尔质量均为44g/mol的化合物甲、乙、丙、丁、戊,均由短周期元素组成。对甲的捕获在降低温室气体排放中具有重要的作用。乙为烃,等物质的量的乙与丁充分燃烧产物为甲与水,且生成水的质量前者是后者的2倍,丙在一定条件下分解获得两种单质,两单质放电时反应生成A,A遇空气变成红棕色气体B。戊是一种极不稳定的物质,在1180℃以下不存在。科学家用质谱仪在工业制硅的反应产物中证实了其存在。
(1)丁的分子式,甲的电子式。
(2)若生成戊的反应中氧化产物与还原产物为同一物质,写出生成戊的化学方程式。
(3)把铁和铜混和物放入一定量B通入水后形成的稀溶液中,反应后过滤,滤出的固体物质投入盐酸中无气体放出,则滤液中一定含有的溶质是。
(4)将0.2mol乙完全燃烧后生成的气体全部缓慢通入300mL某浓度的NaOH溶液中,气体完全被吸收,溶液中NaOH无剩余,则NaOH溶液的浓度为(若有定值则写具体数值,无定值则写范围)。
(5)将等物质的量A、B的混合物溶于NaOH溶液中得到只含有一种溶质的溶液,此溶质的化学式为,设计简单实验方案证明溶液中含有此溶质。
某科研小组从含有较多Ag+、Fe3+、Al3+的工业废水中,按下图所示方法分离和提取金属单质:
已知:实验室甲、乙、丙、丁四种物质只能从氨水、碳酸铵、氢氧化钠、稀硫酸、葡萄糖五种溶液中选择,也可以用这五种溶液来制备。
对该实验分析正确的是
A.金属A、B、C分别为Ag、Fe、Al
B.g、f都为氧化物,工业上均采用电解g与f获得对应金属单质
C.沉淀b为混合物,主要成分为沉淀d和沉淀e
D.甲是氢氧化钠,丁为稀硫酸
芳香烃X是一种重要的有机化工原料,其摩尔质量为92g·mol一1,某课题小组以它为原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。已知A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。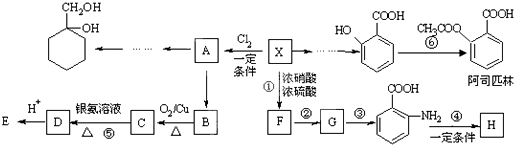
已知:
回答下列问题:
(1)对于阿司匹林,下列说法正确的是_______
| A.是乙酸的同系物 |
| B.能发生酯化反应 |
| C.1 mol阿司匹林最多能消耗2mol NaOH |
| D.不能发生加成反应 |
(2)H的结构简式是_________,F→G的反应类型是_______。
(3)写出C→D的化学方程式_______。
( 4)写出符合下列条件的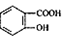 的同分异构体的结构简式_______。(写出2种)
的同分异构体的结构简式_______。(写出2种)
①属于芳香族化合物,且能发生银镜反应;
②核磁共振氢谱图中峰面积之比为1 :2:2:1
③分子中有2个羟基
(5)以A为原料可合成 ,请设计合成路线,要求不超过4步(无机试剂任选)。
,请设计合成路线,要求不超过4步(无机试剂任选)。
注:合成路线的书写格式参照如下示例流程图: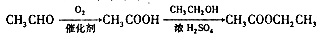
2013年9月,中国华北华中地区发生了严重的雾霆天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染。汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾履形成的原因。
(1)汽车尾气净化的主要原理为;2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0,在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO在t1时刻达到平衡状态。
N2(g)+2CO2(g) △H<0,在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO在t1时刻达到平衡状态。
①能判断该反应达到平衡状态的标志是____。
| A.在单位时问内生成1mol CO2的同时消耗了lmol CO |
| B.混合气体的密度不再改变 |
| C.混合气体的平均相对分子质量不再改变 |
| D.混合气体的压强不再变化 |
②在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件。请在右图中补充画出从t2到t4时刻正反应速率随时间的变化曲线: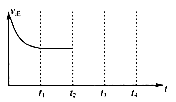
③若要同时提高该反应的速率和NO的转化率,采取的措施有_____、____。(写出2个)
(2)改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气,其反应原理为C(s)+H2O(g) CO(g)+H2(g) △H=+131.3kJ/mol。
CO(g)+H2(g) △H=+131.3kJ/mol。
①该反应在___下能自发进行(填“高温”或“低温”)。
②煤气化过程中产生的有害气体H2S可用足量的Na2C03溶液吸收,该反应的离子方程式为____。(已知:H2S:Ka1=9.1×10-8;Ka2=1.1×10-12。H2CO3:Ka1=4.30×10-7;Ka2=5.61×10-11)
(3)已知反应:CO(g)+H2O(g) CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通人到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通人到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
| 实验 |
温度/℃ |
起始量/mol |
平衡量/mol |
达平衡所需时间/min |
||
| CO |
H2O |
H2 |
CO |
|||
| 1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
| 2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
| 3 |
900 |
a |
b |
c |
d |
t |
①实验1条件下平衡常数K=______(保留小数点后二位)。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是______。
③该反应的△H ______0(填“<”或“>”);若在9000C时,另做一组实验,在此容器中加入l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2,则此时υ正______υ逆(填“<”,“>”,“=”)。