(14 分)碳及其化合物应用广泛。
I.工业上利用CO和水在沸石分子筛表面反应制氢气,CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
(1)向 1L恒容密闭容器中注入CO和H2O(g),830oC时,测得部分数据如下表。
| t/min |
0 |
1 |
2 |
3 |
4 |
5 |
| n(CO)/mol |
0.200 |
0.160 |
0.125 |
0.099 |
0.080 |
0.080 |
| n(H2O)/mol |
0.300 |
0.260 |
0.225 |
0.199 |
0.180 |
0.180 |
则该温度下反应的平衡常数K=
(2)相同条件下,向 1L恒容密闭容器中,同时注入1molCO、1molH2O(g)、2molCO2和2molH2,此时
v(正) v(逆)(填“>”“=”或“<”)
II.已知:CO(g)+1/2O2(g)=CO2(g) △H1=-141kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H2=-484kJ·mol-1
CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g) △H3=-726kJ·mol-1
(3)利用CO、H2化合制得液态甲醇的热化学方程式为
Ⅲ.一种新型氢氧燃料电池工作原理如下图所示。
(4)写出电极A的电极反应式 ,放电过程中,溶液中的CO32-将移向电极 (填A或B)
(5)以上述电池电解饱和食盐水,若生成0.2mol Cl2,则至少需通入O2的体积为 L(标准状况)
(9分)某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物NH3性质的探究。
(1)实验室制取氨气的化学方程式为。
(2)某同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的?(填“能”或“否”),理由是。
(3)该小组的同学设计了如图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性。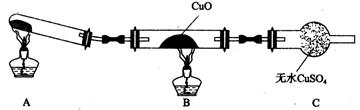
①该装置在设计上有一定缺陷。为保证实验结果的准确性,对该装置的改进措施是
。
②利用改进后的装置进行实验,CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。氨气与CuO反应的化学方程式为。
③有同学认为NH3与CuO反应生成的红色物质中可能含Cu2O。Cu2O在酸性溶液中Cu+歧化生成Cu和Cu2+。请设计一个简单的实验检验该红色物质中是否含有Cu2O
。
(9分)明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下: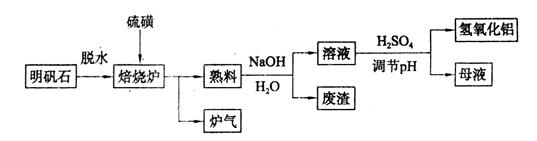
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S 2Al2O3+9SO2,该反应的氧化剂是_______,若生成1 mol Al2O3,则转移的电子数为_______。
2Al2O3+9SO2,该反应的氧化剂是_______,若生成1 mol Al2O3,则转移的电子数为_______。
(2)将标况下1.12L炉气通入100mL 0.5/L NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为_______________ _______。
(3)熟料溶解时反应的离子方程式为___________________________________。
(4)检验废渣中含有Fe2O3所需的试剂是____________。
(5)母液中溶质主要成分的化学式为__________,溶液调节pH后经过滤、洗涤可得Al(OH)3沉淀,证明沉淀已洗涤干净的实验操作和现象是_________________________。
(10分)A、B、C、D、E、F、G七种元素的原子序数依次递增。已知:
①G的原子序数为29,其余的均为短周期主族元素;
②A是宇宙中含量最多的元素,B原子最外层电子数是次外层电子数的2倍,C原子核外有三个未成对电子;
③D和E原子价电子排布式均为ns2np4;④F的单质是黄绿色气体。
请回答下列问题:
(1)G2+的核外电子排布式是。在[G(NH3)4]2+离子中,G2+与NH3分子形成的是键。
(2)与B、C形成的阴离子(BC—)互为等电子体的微粒有、(分子和离子各写一种)。
(3)B与C形成的化合物中,下列判断正确的是。
a.氢化物稳定性:B>C b.氢化物沸点:B<C
c.最高价氧化物的水化物酸性:B<Cd.非金属性:B>C
(4)B、C、D第一电离能由小到大的顺序为(用元素符号作答),B的一种氢化物相对分子质量为26,分子中的σ键与π键数目比为。
(5)七种元素中,电负性最大的元素与B元素形成化合物电子式为,该物质的晶体属于。
松油醇是一种调香香精,它是α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(下式中的18是为区分两个羟基而人为加上去的)经下列反应制得:
(1)α-松油醇的分子式
(2)α-松油醇所属的有机物类别是
(a)醇(b)酚(c)饱和一元醇
(3)α-松油醇能发生的反应类型是
(a)加成(b)水解(c)氧化
(4)在许多香料中松油醇还有少量以酯的形式出现,写出RCOOH和α-松油醇反应的化学方程式。
(5)写结构简式:β-松油醇,γ-松油醇。
X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X原子基态时最外层电子数是其内层电子数的2倍 |
| Y |
Y原子基态时2p原子轨道上有3个未成对的电子 |
| Z |
Z的基态原子最外层电子排布式为:nsnnpn+2 |
| W |
W的原子序数为29 |
(1)基态W原子的价电子排布式是_________________。
(2)X、Y、Z三种元素第一电离能从大到小的顺序是____________。(填化学式)
(3)Y的氢化物分子的空间构型是_______________;该氢化物分子中Y原子轨道的杂化类型是___________。
(4)X的气态氢化物和Y的气态氢化物中沸点高的是,(填化学式)其主要原因是。
(5)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为 ,每个Ba2+与 个O2-配位。