已知A、B、C、D和E都是元素周期表中前36号元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素。D的价电子数为2,D跟B可形成离子化合物,其晶胞结构如图。请回答: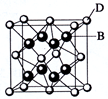
(1)A的元素符号是_____
(2)B与A形成的化合物比C 与A形成的化合物沸点高,其原因是_____
(3)E元素名称是 ;它的+2价离子的电子排布式为_____
(4)从图中可以看出,D跟B形成的离子化合物的化学式为 ;在晶体中与D距离最近且相等的B有 个, D跟B形成的离子化合物的熔点 D跟C形成的离子化合物的熔点(填“>”或“<”)。
向100mL0.1mol/L硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol/L Ba(OH)2溶液.随着Ba(OH)2溶液体积V(横坐标)的变化,沉淀总物质的量n的变化如图所示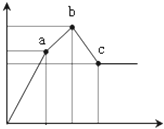
已知铝盐中滴加过量氨水能产生Al(OH)3沉淀,该沉淀遇强碱如NaOH溶液又可溶解。请回答下列问题:
(1)写出b﹣c发生反应的离子方程式:;
(2)下列说法正确的是
| A.a点的溶质为(NH4)2SO4 |
| B.b点溶液中一定存在:c(NH4+)+c(H+)=c(OH﹣) |
| C.b点沉淀为Al(OH)3和BaSO4 |
| D.C点溶液中一定存在:c(AlO2﹣)>c(Ba2+)>c(NH4+) |
(3)写出a﹣b发生反应的离子方程式:;
(4)滴加到c点共加入Ba(OH)2溶液的体积为mL,b、a两点沉淀的质量差为g(精确到0.001).
将Na2O2和NaHCO3的混合物粉末分为两等份,其中一份加入100mL盐酸,充分反应后溶液为中性,放出气(已干燥)2.24L(标准状况),将生成的气体全部通入另一份混合粉末,充分反应后气体的体积变为2.016L(标准状况),问:
(1)2.24L气体的成分为:;
(2)试通过讨论并计算每份混合粉末中Na2O2和NaHCO3的物质的量:
第一种情况:n(Na2O2)=mol和n(NaHCO3)=mol;
第二种情况:n(Na2O2)=mol和n(NaHCO3)=mol.
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
阳离子:K+ Na+Cu2+Al3+
阴离子:SO42-HCO3- OH-Cl-
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸酸化的硝酸钡溶液,只有A中放出无色气体,只有D中产生白色沉淀;
⑤将B、C两溶液混合,未见沉淀或气体生成。根据上述实验填空:
(1)写出B、D的化学式:B____,D。
(2)C可用作净水剂,用离子方程式表示其净水原理_______。
(3)将含0.01 mol A的溶液与含0.02 mol E的溶液反应后,向溶液中滴加0.1 mol·L-1稀盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是

(4)在m mL b mol·L-1C溶液中,加入等体积a mol·L-1的E溶液。
当a≤3b时,生成沉淀的物质的量是mol;
当3b<a<4b件时,生成沉淀的物质的量是mol。
以下是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙为还原性气体,丙为强碱溶液,G为红褐色沉淀,I的颜色呈浅绿色。
(1)若F是由Na+和SO42-组成的溶液,则甲的化学式是 _____________,列举A物质的一种用途______________________________________________________________。
(2)若D是能使澄清石灰水变浑浊的气体,则乙的化学式为________,丁属于单质、酸、碱中的________;在I溶液中加入氢氧化钠溶液,可以观察到的现象是______________________________,
对应的离子方程式和化学方程式依次是______________________,___________________。
(3)写出G→A+C的化学方程式: ___________________________________。
(4)写出E和C反应的方程式并用单线桥法标明电子的转移方向和数目:__________。
(5)若A中混有杂质Al2O3,除去杂质的方法是加入过量的________,该反应的离子方程式为__________。
(6)由E和A组成的混合物与稀H2SO4作用,固体恰好溶解,所得溶液中不含Fe3+,且生成的Fe2+与H2的物质的量之比为4∶1。则反应物中A、E、H2SO4的物质的量之比为________。
已知A、B、C、D、E、F、G为中学化学中常见的化合物,其中A是淡黄色固体,B是无色液体,G为红褐色沉淀。常温下甲、乙、丙为气态非金属单质,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如下图所示(有的反应部分产物已经略去)。请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A,E,戊。
(2)F转化为C的过程中出现的现象是:。
(3)写出②中反应的离子方程式:。
(4)①~⑥转化中不含有氧化还原反应的是:(填序号)。